
Henrique Santiago Baltar Pazos1; Paula Fernanda Morais Ramalho Baltar Pazos1; Pedro Antônio Nogueira Filho1; Ana Beatriz Diniz Grisolia1; André Berger Emiliano Silva1; José Álvaro Pereira Gomes1
DOI: 10.1590/S0004-27492011000300010
RESUMO
OBJETIVO: Relatar os resultados da ceratoplastia endotelial com desnudamento da Descemet (DSEK) utilizando o dispositivo TAN EndoGlideTM para facilitar a introdução da membrana endotelial. MÉTODOS: Série de casos consecutivos, prospectiva. Foram incluídos 9 pacientes com edema corneano secundário à disfunção endotelial. Melhor acuidade visual corrigida, refração, astigmatismo ceratométrico, espessura corneana central, densidade das células endoteliais e complicações foram analisadas após seguimento de seis meses. RESULTADOS: Houve melhora do edema de córnea e da visão em 7 pacientes (77,78%). A melhor acuidade visual corrigida ficou entre 20/40 e 20/200. A densidade endotelial média após 6 meses variou entre 1.305 céls/mm² e 2.346 céls/mm² com média de perda de 33,14%. Desprendimento de parte do enxerto ocorreu em 1 olho (11,11%), falência primária do transplante endotelial em 2 olhos (22,22%). CONCLUSÃO: O dispositivo TAN EndoGlideTM facilita a introdução do enxerto na ceratoplastia endotelial com desnudamento da Descemet.
Descritores: Transplante de córnea; Edema de córnea; Perda de células endoteliais da córnea; Lâmina limitante posterior da córnea; Ceratoplastia endotelial com remoção da membrana de Descemet
ABSTRACT
PURPOSE: To report the results of Descemet stripping endothelial keratoplasty (DSEK) using the TAN EndoGlideTM device to facilitate the insertion of the endothelial membrane. METHODS: Prospective clinical study that included nine patients presenting corneal edema secondary to endothelial dysfunction. Best corrected visual acuity, refraction, central corneal thickness, endothelial cell density and complications were analyzed after a six-month follow-up. RESULTS: There was a significant improvement in the corneal edema and visual acuity in 7 patients (77.78%). The best corrected visual acuity ranged between 20/40 and 20/200. The average density of endothelial cells in six months varied between 1,305 cells/mm² and 2,346 cells/mm² with an average loss of 33.14% cells. Detachment of part of the graft was observed in one eye (11.11%) and primary failure of the endothelial transplantation occurred in 2 eyes (22.22%). CONCLUSION: The device TAN EndoGlideTM facilitates the introduction of the graft in Descemet stripping endothelial keratoplasty.
Keywords: Corneal transplantation; Corneal edema; Corneal endothelial cell loss; Descemet membrane; Descemet stripping endothelial keratoplasty
INTRODUÇÃO
A córnea é um tecido transparente que contribui com 74% do poder dióptrico do olho. Esta transparência ocorre, principalmente, devido ao controle da hidratação pelo endotélio, realizado pelo sistema de transporte iônico controlado pela enzima Na+/K+ - ATPase. A disfunção endotelial, encontrada em afecções como distrofia de Fuchs e ceratopatia bolhosa do afácico ou pseudofácico, reduzem a eficácia da bomba metabólica endotelial resultando em edema e perda de visão(1).
As células do endotélio humano raramente se proliferam in vivo. Devido a esta falta de capacidade proliferativa, o tratamento mais comumente preconizado nos casos de disfunção endotelial com perda de transparência da córnea é a ceratoplastia penetrante (PK)(2,3). Esta técnica, realizada com o olho aberto, tem como desvantagem maior risco de complicação intraoperatória, maior chance de rejeição ou infecção e pode induzir astigmatismo alto e irregular comprometendo a qualidade visual final(4).
Em 1998, Melles et al., descreveram técnica de transplante de disco lamelar composto por estroma profundo e endotélio (PLK) em humanos, implantado por uma incisão escleral de 9,0 mm, que é suturada posteriormente(5-7). Esta técnica se popularizou nos Estados Unidos a partir de 2001 como ceratoplastia endotelial lamelar profunda (DLEK)(5-8). As vantagens do DLEK incluem: recuperação rápida da visão, indução mínima de astigmatismo e boa acuidade visual final mesmo com a permanência do estroma do receptor. No entanto, o DLEK necessita de instrumental cirúrgico específico e requer grande habilidade cirúrgica(9,10). Em 2003, Melles et al., introduziram um avanço na técnica de transplante endotelial: a descemetorrexis, que consistia no desnudamento da membrana de Descemet e endotélio do receptor, preservando o estroma profundo (Descemet stripping endothelial keratoplasty - DSEK)(6,11,12).
Esse avanço tornou a técnica mais acessível e diminuiu o tempo cirúrgico. Após estudo publicado por Price em 2006, que incluiu 200 olhos submetidos a DSEK, esta técnica ganhou muitos adeptos e praticamente substituiu o DLEK(2,12).
A preparação do tecido doador foi facilitada com a utilização do microcerátomo. Esta variação da técnica foi denominada de ceratoplastia endotelial com desnudamento automatizado da Descemet (DSAEK)(2). Mais recentemente, alguns serviços têm utilizado o laser de femtosegundo para a confecção do tecido doador(13).
Um dos maiores desafios dos procedimentos de transplante endotelial é a introdução do enxerto de maneira mais atraumática possível para não haver perda do número de células endoteliais(14,15). Mais recentemente, uma série de injetores e insertores têm sido desenvolvidos para facilitar a introdução do enxerto(14-18).
DSAEK ou DSEK são considerados em muitos países como tratamento de escolha para disfunção endotelial devido à rápida recuperação visual, maior estabilidade de refração e menor risco cirúrgico quando comparado ao transplante penetrante (PK)(2,12).
Uma das desvantagens desta técnica é a perda endotelial significantemente maior em um a dois anos em comparação ao PK(12). Alguns autores, em estudos prospectivos sobre DSEK/DSAEK (n=80 olhos e n=263 olhos, respectivamente), demonstraram que houve 34% de perda de células do endotélio em seis meses e 35% em um ano(17,19). Essa perda de células endoteliais pode ser explicada possivelmente pela curva aprendizado do DSEK/DSAEK e principalmente por fatores relacionados ao preparo e manipulação do botão doador(17,19,20).
Atualmente, para solucionar estes problemas, cirurgiões e empresas de equipamento cirúrgico oftalmológico, em conjunto, têm desenvolvido dispositivos para inserção do tecido doador, com o intuito de evitar a compressão exercida pela ferida cirúrgica ao enxerto e minimizar o dano endotelial(2). Entre os mais utilizados atualmente estão os insertores: Busin Glide (DSAEK Busin Glide Spatula, Moria SA, Antony, Fr) e TAN EndoGlideTM. Entre os injetores temos: Endosaver (Endosaver, Ocular Systems, INC., Winston-Salem, EUA) e o Neusidl Corneal Inserter (Neusidl Corneal Inserter, Fischer Surgical, Arnold, EUA).
Outros autores em 2008 comprovaram que ao dobrar o enxerto em forma de taco há uma perda de 32% de células endoteliais. Entretanto, ao enrolá-lo sem que ocorra contato endotélio-endotélio, a perda endotelial reduz-se a um terço, chegando a 8%(17).
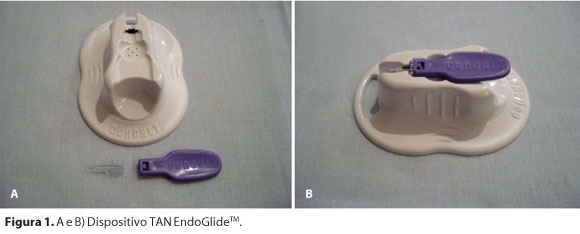
O objetivo deste trabalho é relatar os resultados do DSEK utilizando o dispositivo TAN EndoGlideTM (Coronet Tan EndoGlide, Network Medical Products Ltd., North Yorkshire, GB) para facilitar a introdução da membrana endotelial (Figura 1).
MÉTODOS
Este estudo foi aprovado pelo Comitê de Ética do Instituto Suel Abujamra. Foram selecionados para esse estudo pacientes apresentando edema corneano secundário à disfunção endotelial devido à distrofia de Fuchs ou ceratopatia bolhosa do pseudofácico ou afácico, com edema persistente, sem melhora com o tratamento clínico, por mais de seis meses. Todos os pacientes assinaram o termo de consentimento para serem submetidos à DSEK com o uso do dispositivo TAN EndoGlideTM. Critérios de exclusão incluíram olhos com inflamação ativa, óleo de silicone na cavidade vítrea, sinéquias anteriores extensas e glaucoma não controlado.
Na avaliação pré-operatória foram avaliadas: melhor acuidade visual corrigida utilizando a Tabela de Snellen, pressão intraocular, biomicroscopia e paquimetria. Dados da córnea doadora como a densidade das células endoteliais, idade do doador, tempo de enucleação e preservação foram fornecidos pela Central Única de Transplantes.
Durante o período pós-operatório (PO), os pacientes foram avaliados nos seguintes dias: 1º PO, 7º PO, 15º PO, 30º PO, 90º PO e 180º PO. Nessas avaliações, foram realizadas: medida da melhor acuidade visual corrigida, biomicroscopia e tonometria. No 30º PO, 90º PO e 180º PO também foram realizados topografia corneana computadorizada (Eye Sys system 2000®, Eye Sys Technologies, Houston, EUA), paquimetria ultrassônica (AccuPachV®, Accutome Inc.Malvern, Filadélfia, EUA) e microscopia especular (Konan®; Noncon Robo-CA-ICO-NAN Inc,. Hyogo, Japão).
Preparo do enxerto endotélio do doador: A córnea doadora foi montada em uma câmara anterior artificial (Barron Artificial Anterior Chamber; Katena Products, Inc. Nova Jersey, EUA). Foi feita marcação da trepanação central, variando de 8,0 a 8,25 mm. Em seguida, foi realizada incisão límbica de 5,0 mm com bisturi de diamante. Foi realizada dissecção lamelar manual, com lâmina crescente e espátula, em aproximadamente dois terços de profundidade da espessura total da córnea. Após a completa dissecção da córnea, o tecido doador, com o endotélio voltado para cima, foi transferido para a base de teflon para ser trepanada. Após a trepanação, a córnea doadora foi submergida em Optisol GS até o preparo do leito receptor.
Preparação do enxerto no injetor TAN EndoGlideTM: Primeiramente, o enxerto foi colocado, na base do dispositivo, com o endotélio para cima. Uma pequena quantidade de viscoelástico dispersivo foi aplicada na superfície endotelial. O injetor foi posicionado na base de preparação e algumas gotas de solução salina balanceada (BSS) foram injetadas para lubrificação. Uma pinça específica, atraumática, desenvolvida por Tan (Coronet Tan EndoGlide Loading Forceps, Network Medical Products Ltd., North Yorkshire, GB.), foi introduzida através do cartucho para segurar a borda do estroma posterior da lentícula doadora. Ao puxar o enxerto para dentro do dispositivo, as bordas se enrolam simetricamente em uma configuração sem que as superfícies endoteliais se toquem. O injetor foi removido da base, rodado para cima, ficando pronto para inserção.
Técnica cirúrgica do DSEK: Peritomia conjuntival temporal foi confeccionada e em seguida foi feito túnel corneoescleral temporal de 5,0 mm. Foram utilizadas três paracenteses corneanas de aproximadamente 1,0 mm cada: uma para colocação de mantenedor de câmara anterior (CA), outra para "Descemetorrexis" e a terceira para colocação do TAN EndoForceps (Coronet TAN EndoGlide Placement Forceps, Network Medical Products Ltd., North Yorkshire, GB.). Com o mantenedor da CA funcionando, o EndoGlideTM foi cuidadosamente inserido através do túnel escleral, garantindo sua introdução completa e oclusão da ferida cirúrgica. O EndoForcepsTM foi introduzido através da paracentese nasal até a plataforma do injetor. Em seguida, a pinça foi posicionada para apreender o estroma e puxar o enxerto. Neste momento, o cartucho foi removido. Mantendo a pinça apreendida com o enxerto, uma pequena quantidade de ar foi introduzida debaixo do botão para evitar a descida para a íris, e, em seguida o botão foi liberado. A ferida escleral foi suturada com três pontos de nylon 10.0, o mantenedor do CA foi removido e as paracenteses foram suturadas, quando necessário. O enxerto foi reposicionado deslizando repetidamente a espátula de íris sobre a córnea. Em seguida, injetou-se mais ar na CA, fazendo com que o tecido doador aderisse à superfície posterior da córnea. A compressão do ar foi mantida por pelo menos 10 minutos, período durante o qual a conjuntiva foi suturada e injeção subconjuntival de antibiótico e esteróide foi aplicada. Finalmente, BSS foi injetado e um pouco de ar foi removido para deixar para trás uma bolha de ar que se aproximasse do tamanho do botão doador. O procedimento foi concluído com colocação de uma lente de contato terapêutica.
DADOS PRÉ-OPERATÓRIOS
Foram incluídos neste estudo 9 olhos de 9 pacientes, sendo 6 (66,67%) olhos direitos e 3 (33,33%) olhos esquerdos. Dos 9 pacientes estudados, 5 (55,56%) eram do sexo feminino e 4 (44,44%) do sexo masculino. A idade média dos pacientes foi de 71,89 anos, variando entre 51 e 87 anos (desvio-padrão 11,37).
Em relação à doença de base (Tabela 1), 7 (77,78%) eram pacientes com ceratopatia bolhosa do pseudofácico ou afácico, 1 (11,11%) paciente apresentava distrofia de Fuchs e 1 (11,11%) paciente apresentava descolamento de Descemet por iatrogenia no procedimento de facoemulsificação. Como outros diagnósticos associados ao quadro, 1 paciente (11,11%) apresentava glaucoma, 1 (11,11%) buraco de mácula, 1 (11,11%) retinopatia diabética, 1 (11,11%) sequela de oclusão venosa do ramo temporal superior e 1 (11,11%) ambliopia.
RESULTADOS
No período pré-operatório, os exames realizados revelaram: melhor acuidade visual de conta-dedos em 7 (77,78%) casos e de percepção de movimento de mãos em 2 (22,22%). Os achados biomicroscópicos foram: edema de córnea em todos os casos (100%), dobras de Descemet em todos os olhos (100%), bolhas epiteliais ou subepiteliais em 6 (66,67%), guttata e catarata em 1 (11,11%) olho, afacia em 1 (11,11%) olho, pseudofacia em 7 (77,78%) olhos e corectopia em 4 (44,44%) dos olhos.
Nesse período, em todos os casos, o aparelho de paquimetria não conseguiu realizar a medida da espessura corneana. Da mesma forma, não foi possível determinar a contagem de células endoteliais pelo aparelho de microscopia especular.
A maioria dos casos desse estudo apresentava no pré-operatório edema importante da córnea com irregularidade da superfície. Sendo assim, apesar de ter sido realizada, ou pelo menos tentada, não conseguimos dados confiáveis nas tonometrias. Com relação às topografias pré-operatórias, em nenhum dos pacientes houve leitura da ceratometria.
Com relação aos pacientes doadores das córneas transplantadas, a idade média foi de 59 anos (variando de 48 a 65 anos, desvio-padrão 6,51). A média da contagem de células endoteliais das córneas doadoras foi 2587,81 céls/mm², variando entre 2262-2898 céls/mm², desvio-padrão 236,92. A média do tempo de preservação foi de 8,11 dias (variando de 6 a 11 dias, desvio-padrão 1,52).
DADOS PÓS-OPERATÓRIOS
No primeiro dia de pós-operatório, todos os olhos apresentaram edema corneano, variando de 2 a 3+ em 4+ e, aparentemente, todos os enxertos estavam aderidos ao estroma posterior do receptor. Após uma semana, houve diminuição do edema corneano evidenciada na biomicroscopia pela melhora da transparência da córnea e redução das dobras de Descemet, que possibilitaram melhor observação dos detalhes da CA. Somente no olho afácico notou-se o desprendimento de parte do enxerto, que foi submetido a uma reintervenção com aplicação de bolha de ar na CA, obtendo resultado satisfatório. No 42º pós-operatório, um dos pacientes permanecia com pequena quantidade de Seidel provocado e foi submetido à ressutura da incisão do túnel corneoescleral.
Durante o período de acompanhamento, 7 (77,78%) pacientes apresentaram melhora da acuidade visual. A melhor acuidade visual corrigida ficou entre 20/40 e 20/200, conforme a tabela 1. Seis pacientes tiveram como resultado refracional hipermetropia e, um paciente apresentou miopia. O astigmatismo variou entre -0,75 e -3,75 dioptrias. Falência do transplante endotelial ocorreu em 2 (22,22%), sendo impossível a avaliação do resultado refracional com a técnica apresentada nesses pacientes.
Em relação aos aspectos biomicroscópicos, com exceção dos dois pacientes que tiveram falência primaria, houve melhora significativa do edema de córnea com total transparência desta. Em 2 olhos (22,22%) houve a formação de pequena sinéquia anterior em região temporal, sendo que um evoluiu com corectopia.
A paquimetria, no sexto mês de pós-operatório, variou entre 504 µm e 764 µm, com média de 638,14 µm.
A última contagem de células endoteliais (Tabela 2), realizada antes da publicação desse estudo, variou entre 1.305 céls/mm² e 2.346 céls/mm², com média de perda de células endoteliais de 33,14%.
Os dois pacientes que apresentaram falência primária do transplante endotelial tiveram o diagnóstico confirmado por volta do terceiro mês de pós-operatório e foram considerados como tendo insucesso. Um deles foi submetido a transplante penetrante de córnea. O outro paciente não quis realizar novo procedimento cirúrgico, estando apenas em acompanhamento clínico no setor de córnea.
DISCUSSÃO
Tan, no VI Congresso Mundial de Córnea (VI WCC Boston 2010), atualizou seus resultados com o EndoGlide em 17 olhos submetidos a DSAEK. Houve perda endotelial de 15,7% em seis meses. Outros estudos revelaram perda de células endoteliais entre 24 a 28% com o mesmo período de acompanhamento utilizando o Busin Glide.
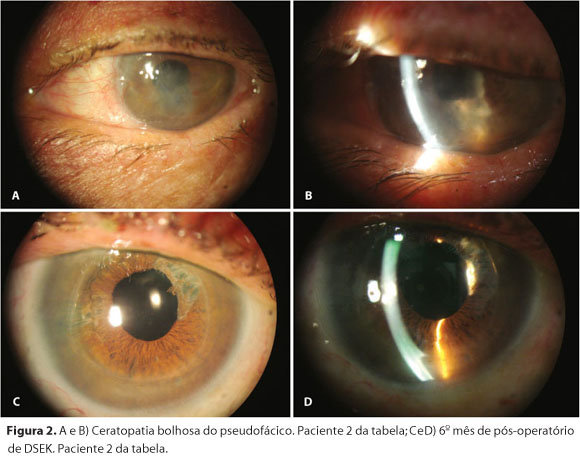
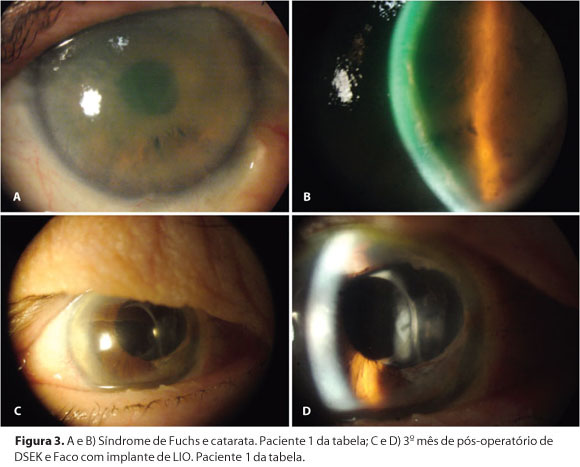
No presente estudo, a perda endotelial dos pacientes que foram acompanhados por um período maior ou igual a 6 meses, foi de 33,14%. A curva de aprendizado com o procedimento e a dissecção manual da córnea doadora podem explicar a maior perda de células endoteliais em comparação com os resultados obtidos por Tan. Além disso, diferentemente da casuística de Tan, que é baseada principalmente em pacientes com distrofia de Fuchs, 7 dos 9 casos por nós operados (77,78%) eram de ceratopatia bolhosa do pseudofácico ou afácico, muitos deles secundários às cirurgias complicadas e apresentando alteração do segmento anterior (Figuras 2 e 3).
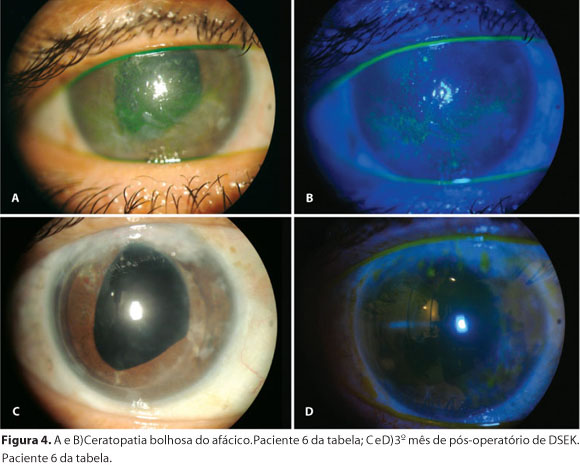
Lee et al., ao revisarem a literatura científica sobre os resultados obtidos com a técnica DSEK/DSAEK, verificaram que a complicação mais comumente relatada é o desprendimento do enxerto na CA. (média 14%)(21). No nosso estudo, verificamos essa ocorrência em apenas um olho (11,11%), que era afácico (Figura 4). O desprendimento foi parcial e facilmente resolvido após nova aplicação de ar na CA. Segundo Rose et al, olhos afácicos são mais sujeitos a este tipo de complicação devido à migração da bolha de ar para o segmento posterior(6).
Segundo a literatura, cerca de 10% dos EK que utilizam a técnica do desnudamento da Descemet cursam com rejeição do botão doador(21). Em nosso estudo, até o momento, não se observou nenhum caso de rejeição. Todavia, falência primária endotelial ocorreu em dois olhos (22,2%), o que coincide com a literatura (média 5%; variando 0%-29%)(2). Correlacionamos o ocorrido à dissecção lamelar manual do enxerto doador, que induz maior traumatismo do endotélio quando comparado à dissecção automatizada ou com o femtosegundo.
Nos procedimentos lamelares posteriores, devido à inserção de tecido, a espessura da córnea aumenta, levando a redução do espaço na CA e a indução de hipermetropia(3,21). No nosso estudo, 8 dos 9 pacientes (88,89%), apresentaram hipermetropia leve, o que coincide com os dados da literatura. O único caso em que houve miopia foi no olho submetido à cirurgia combinada [facoemulsificação com implante de lente intraocular (LIO) e DSEK]. Nesse caso, devido às alterações importantes provocadas pela distrofia de Fuchs na córnea, a biometria foi estimada através dos dados do olho contralateral, previamente submetido a um transplante penetrante corneano.
A melhora da acuidade visual foi observada nos primeiros meses após a realização do DSEK. Segundo a literatura, a melhora da acuidade visual após o transplante penetrante de maneira semelhante a de um transplante endotelial ocorre de maneira mais lenta, após cerca de 2 a 3 anos(23).
Dos 9 pacientes estudados, 5 apresentavam condições para limitação da recuperação visual, como ambliopia, buraco macular, retinopatia diabética, glaucoma e sequela de oclusão do ramo temporal superior. Entre os 5, 2 evoluíram com falência primária e, portanto, as limitações por eles apresentadas não interferiram nos resultados.
O transplante endotelial é uma mudança revolucionária no tratamento de distúrbios endoteliais, evitando a realização do transplante penetrante, que é mais invasivo.
Os cirurgiões têm desenvolvido melhorias na técnica do transplante endotelial nos últimos anos, mas não conseguiram chegar a um consenso com relação ao método ideal para transferência do tecido.
O insertor TAN EndoGlideTM utilizado nesse estudo facilita a técnica cirúrgica do DSEK mesmo nos casos de ceratopatia bolhosa do pseudofácico que apresentam alterações na CA.
Mais estudos comparativos são necessários para determinar se a perda endotelial é menor com o dispositivo TAN EndoGlideTM em comparação com outros insertores.
REFERÊNCIAS
1. Klyce SD, Beuerman RW. Structure and function of the cornea. In: Kaufman HE, Barron BA, McDonald MB, editors. The cornea. 2th ed. New York: Butterworth-Heinemann; 1998. p.3-50.
2. Ide T. Descemet´s stripping automated endothelial keratoplasty injecting device. Expert Rev Ophthalmol. 2009; 4(1):5-9.
3. Basak SK. Descemet stripping and endothelial keratoplasty in endothelial dysfunctions: three-month results in 75 eyes. Indian J Ophthalmol. 2008g;56(4):291-6.
4. Shih CY, Ritterband DC, Rubino S, Palmiero PM, Jangi A, Liebmann J, et al. Visually significant and nonsignificant complications arising from Descemet stripping automated endothelial keratoplasty. Am J Ophthalmol. 2009;148(6):837-43.
5. Dapena I, Ham L, Lie J, Van-Der-Wess J, Melles GR. [Descement membrane endothelial keratoplasty (DMEK): two-year results.] Arch Soc Esp Oftalmol. 2009;84(5):237-43. Spanish.
6. Rose L, Kelliher C, Jun AS. Endothelial keratoplasty: historical perspectives, current techniques, future directions. Can J Ophthalmol. 2009;44(4):401-5.
7. Melles GR, Eggink FA, Lander F, Pels E, Rietveld FJ, Beekhuis WH,, et al. A surgical techinique for posterior lamellar keratoplasty. Cornea. 1998;17(6):618-26.
8. Terry MA, Ousley PJ. Small-incision deep lamellar endothelial keratoplasty (DLEK): six-month results in the first prospective clinical study. Cornea. 2005;24(1):59-65.
9. Terry MA, Ousley PJ. In pursuit of emmetropia: spherical equivalent refraction results with deep lamellar endothelial keratoplasty (DLEK). Cornea. 2003;22(7):619-26.
10. Terry MA, Ousley PJ. Rapid visual rehabilitation after endothelial transplants with deep lamellar endothelial keratoplasty (DLEK). Cornea. 2004;23(2):143-53.
11. Melles GR, Wijdh RH, Nieuwendaal CP. A technique to excise the descemet membrane from a recipient cornea (descemetorhexis). Cornea. 2004;23(3):286-8.
12. Price FW,Jr., Price MO. Descemet´s stripping with endothelial keratoplasty in 200 eyes: early challenges and techniques to enhance donor adherence. J Cataract Refract Surg. 2006;32(3):411-8.
13. Cheng YY, Hendrikse F, Pels E, Wijdh RJ, van Cleynenbreugel H, Eggink CA, et al. Preliminary results of femtosecond laser-assisted descemet stripping endothelial keratoplasty. Arch Ophthalmol. 2008;126(10):1351-6.
14. Walter KA, Foster JB. Innovation in endothelial keratoplasty, early results from a no-fold, small-incision, DSAEK graft injector. Cataract Refract Surg Today. 2009; Sept: 83-5.
15. Busin M, Bhatt PR, Scorcia V. A modified technique for Descemet membrane stripping automated endothelial keratoplasty to minimize endothelial cell loss. Arch Ophthalmol. 2008;126(8):1133-7. Comment in: Arch Ophthalmol. 2008;126(8):1140.
16. Mehta JS, Por YM, Poh R, Beuerman RW, Tan D. Comparison of donor insertion techniques for descemet stripping automated endothelial keratoplasty. Arch Ophthalmol. 2008;126(10):1383-8.
17. Terry MA, Chen ES, Shamie N, Hoar KL, Friend DJ. Endothelial cell loss after Descemet's stripping endothelial keratoplasty in a large prospective series. Ophthalmology. 2008; 115(3):488-96.
18. Bahar I, Kaiserman I, Sansanayudh W, Levinger E, Rootman DS. Busin guide vs forceps for the insertion of the donor lenticule in Descemet stripping automated endothelial keratoplasty. Am J Ophthalmol. 2009;147(2):220-6. Comment in: Am J Ophthalmol. 2009;148(1):175; author reply 175-6.
19. Price MO, Price FW Jr. Endothelial cell loss after descemet stripping with endothelial keratoplasty influencing factors and 2-year trend. Ophthalmology. 2008;115(5):857-65. Comment in: Ophthalmology. 2009;116(3):367-8.
20. Lee WB, Jacobs DS, Musch DC, Kaufman SC, Reinhart WJ, Shtein RM. Descemet´s stripping endothelial keratoplasty: safety and outcomes: a report by the American academy of ophthalmology. Ophthalmology. 2009;116(9):1818-30.
21. Yoo SH, Kymionis GD, Deobhakta AA, Ide T, Manns F, Culbertson WW, et al. One-year results and anterior segment optical coherence tomography findings of descemet stripping automated endothelial keratoplasty combined with phacoemulsification. Arch Ophthalmol. 2008;126(8):1052-5.
22. Hjortdal J, Ehlers N. Descemet's stripping automated endothelial keratoplasty and penetrating keratoplasty for Fuchs' endothelial dystrophy. Acta Ophthalmol. 2009;87(3):310-4.
Correspondence address:
José Álvaro Pereira Gomes
Rua Sabará, 566 - Cj. 43
São Paulo - SP
01239-010 - Brazil
E-mail: [email protected]
Submitted for publication: August 9, 2010
Accepted for publication: May 9, 2011
Study carried out at the Instituto Suel Abujamra - ISA - São Paulo (SP), Brasil.
Funding: No specific financial support was available for this study.
Disclosure of potential conflicts of interest: H.S.B.Pazos, None; P.F.M.R.B.Pazos, None; P.A. Nogueira Filho, None; A.B.D.Grisolia, None; A.B.E.Silva, None; J.A.P.Gomes Consultant (Alcon, Allergan, Bausch & Lomb), Speaker (Alcon, Allergan, Bausch & Lomb).