Arq. Bras. Oftalmol. 2011; 74 (1): 10.1590/S0004-27492011000100011
Total: 1975
Glauco Henrique Reggiani Mello1; Fabíola Grigoletto Lupion1; Fernanda Moreira Oliveira1; Lucas Roskamp Bude2; Daniel Wasileweski1; Teresa Cristina Cavalcanti1; Hamilton Moreira1
DOI: 10.1590/S0004-27492011000100011
RESUMO
OBJETIVOS: Avaliar a ação do bevacizumabe subconjuntival em modelo experimental de neovascularização em córnea de coelho. Analisar se o modelo de avaliação empregado é adequado e comparar entre os grupos a extensão dos vasos, inflamação e re-epitelização da córnea. MÉTODOS: Estudo experimental, prospectivo em 20 coelhos submetidos a trauma químico com hidróxido de sódio a 1 N divididos em dois grupos, Imediatamente após a queimadura, o grupo tratado recebeu injeção subconjuntival de 0,15 ml (3,75 mg) de bevacizumabe e o grupo controle, injeção subconjuntival de 0,15 ml de soro fisiológico a 0,9%. Após 25 dias, foi realizada análise fotográfica digital para avaliar a extensão e inflamação/calibre dos vasos segundo critério pré-estabelecido e estudo histopatológico da córnea, no qual foi avaliado o estado do epitélio e o número de polimorfonucleares. RESULTADOS: A extensão dos neovasos corneanos foi menor no grupo estudo em relação ao controle (p<0,001). Não houve diferença significativa entre os grupos na inflamação/calibre dos vasos. A análise histopatológica mostrou que não ocorreu diferença entre os grupos nas variáveis estado do epitélio e número de polimorfonucleares. A análise de concordância para a variável extensão dos vasos e para a variável inflamação/calibre dos vasos teve uma estimativa do coeficiente de Kappa respectivamente de 0,705 e 0,500 indicando bom grau de concordância nas diferentes avaliações cegadas, validando o método empregado. CONCLUSÕES: O modelo de avaliação foi adequado e pode ser reproduzido para avaliar outras drogas na córnea. O bevacizumabe inibiu a neovascularização corneana, porém não foi eficaz em reduzir o processo inflamatório. A droga não atrasou a re-epitelização da córnea.
Descritores: Neovascularização patológica; Neovascularização da córnea; Inibidores da angiogênese; Queimaduras químicas; Modelos animais de doença
ABSTRACT
PURPOSES: To evaluate the effect of subconjunctival bevacizumab in an experimental model of neovascularization in rabbit cornea. Determine its effect on vessels extension, inflammation, epithelialization of the cornea and whether the evaluation method used is appropriate to compare neovascular models. METHODS: Experimental, prospective, randomized, blinded study in twenty rabbits subjected to chemical trauma with sodium hydroxide at 1N divided into two groups. The study group received subconjunctival injection of 0.15 ml (3.75 mg) of bevacizumab and was compared with the control group that received subconjunctival injection of 0.15 ml saline solution. After 25 days, digital photographic analysis was performed to assess the vessel's extension and inflammation/diameter according to pre-established criteria. Histopathology of the cornea, which evaluated the state of the epithelium and the number of polymorphonuclear cells was also studied. RESULTS: The length of the neovessels was greater in the control group compared to the study group (P=<0.001). There was no difference in inflammation/vessel diameter between groups. Histopathology analysis showed that there was no difference between groups for the variables state of the epithelium and number of polymorphonuclear cells. The concordance analysis for the variable extension of the vessels and the variable inflammation/vessel diameter was estimated with Kappa coefficients of 0.705 and 0.500 respectively, indicating a good level of agreement in different evaluations and validating the method. CONCLUSIONS: The experimental model is adequate and can be reproduced to evaluate other drugs in the cornea. Bevacizumab inhibit the neovessels' growth but was not effective in preventing the inflammatory response. The drug did not delay the reepithelialization of the cornea.
Keywords: Neovascularization, pathological; Corneal neovascularization; Angiogenesis inhibitors; Burns, chemical; Diseases models, animal
INTRODUÇÃO
Trauma ocular, infecção, inflamação e degeneração são responsáveis por neovascularização da córnea. Os neovasos apresentam alterações estruturais que permitem extravasamento do fluido para o espaço extravascular, estase sanguínea e hemorragia, ocasionando diminuição da transparência corneana com progressiva redução da visão(1-2). Neovasos corneanos são fatores de risco para rejeição no transplante de córnea(3), devido ao favorecimento no acesso de células apresentadoras de antígenos ao tecido doador.
Atualmente, os corticóides têm sido a primeira escolha no tratamento da neovascularização corneana devido ao seu alto poder de diminuir o processo inflamatório(4) e a proliferação vascular que se inicia após a cascata inflamatória(5). Entretanto, apesar do corticóide ser utilizado em várias doenças oculares neovasculares, o seu modo de ação inespecífico é responsável por uma alta incidência de efeitos adversos (retardo no processo de cicatrização, glaucoma e catarata(6-7)).
Expressão intensa de fator de crescimento do endotélio vascular (VEGF) é encontrada em córneas humanas neovascularizadas ou expostas a queimaduras por álcali(8-9). Estudos recentes correlacionam o VEGF e seus receptores em múltiplas doenças oculares neovasculares (retinopatia diabética(10), neovascularização da íris(11), neovascularização da degeneração macular relacionada à idade(12) e neovascularização da córnea(8)).
O bevacizumabe (inibidor do VEGF) é utilizado para tratamento de doenças de retina desde 2005, com estudos mostrando que a droga é segura para o uso ocular(13). As drogas anti-VEGF, como o bevacizumabe, têm provocado uma revolução no tratamento das doenças neovasculares, não só por reduzir os vasos sanguíneos, como também pela sua suposta ação nos fibroblastos(14).
O bevacizumabe possui efeitos benéficos na neovascularização da degeneração macular relacionada à Idade (DMRI), na retinopatia diabética e no glaucoma. Esses efeitos podem ser estendidos para a redução da formação de neovasos em outras regiões do globo ocular. Com isso em mente nos propusemos a avaliar sua ação na córnea.
O objetivo do trabalho é avaliar a neovascularização em modelo experimental de córnea de coelhos, 25 dias após trauma químico com NaOH, comparando coelhos que receberam injeção subconjuntival de bevacizumabe com aqueles que receberam soro fisiológico. Analisar se o modelo de avaliação empregado é adequado e reprodutível.
MÉTODOS
Estudo experimental, prospectivo e comparativo desenvolvido no Instituto de Pesquisas Médicas do Programa de Pós-Graduação em Princípios de Cirurgia da Faculdade Evangélica do Paraná e do Hospital Universitário Evangélico de Curitiba. Foram respeitadas as Normas e Princípios na Experimentação Animal.
Foram estudadas 20 córneas de 20 coelhos da linhagem Nova Zelândia, albinos, machos, sadios, com peso entre 2.300 a 2.500 g e entre 3 e 4 meses de vida. Provenientes do Instituto de Tecnologia do Paraná.
Todos os animais foram examinados antes do início do experimento para verificar a higidez da córnea.
Os animais foram divididos aleatoriamente em dois grupos de 10 coelhos cada (grupo controle e estudo) utilizando o programa Reseach Randomizer® (www.randomizer.org). O investigador que estava realizando os procedimentos não tinha conhecimento da randomização.
Os coelhos foram anestesiados com cloridrato de xilazina (0,1 ml/kg) e cloridrato de ketamina (0,2 ml/kg) intramuscular, para o procedimento de queimadura e da injeção subconjuntival da córnea.
Após o procedimento anestésico, os animais foram submetidos à queimadura corneana do olho direito com hidróxido de sódio (NaOH) a 1 N(15), embebido em papel filtro com 3 mm de diâmetro, aplicado durante 20 segundos na córnea superior tangencial porém sem contato direto com o limbo(16). Após o procedimento, a córnea foi irrigada com 20 ml de soro fisiológico a 0,9%.
Os animais grupo controle receberam injeção subconjuntival com 0,15 ml de solução salina isotônica a 0,9%. O grupo estudo recebeu injeção subconjuntival de 0,15 ml (3,75 mg) de bevacizumabe (Avastin®, Roche AG, Basel - Suíça). As injeções foram aplicadas imediatamente após a queimadura corneana.
Os animais foram novamente anestesiados após 25 dias da queimadura química sendo utilizado o mesmo procedimento anestésico descrito anteriormente. Após a sedação os coelhos foram posicionados adequadamente e imobilizados para a realização de fotografias digitais.
As variáveis estudadas foram extensão dos vasos, grau de inflamação/calibre dos vasos, integridade do epitélio e número de polimorfonucleares.
Utilizou-se câmera Sony Cybershot 7.2 megapixels (Sony Corporation, Tóquio - Japão) e lente acessória Zeiss (Carl Zeiss AG, Oberkochen - Alemanha) com magnificação de 40 vezes em distância de 5 cm. A máquina fotográfica foi apoiada em tripé fixo. Na sequência, foi colocado blefarostato no olho direito para melhor apresentação da córnea, da área queimada e da neovascularização. As fotografias foram realizadas em posição frontal.
Foram realizadas duas avaliações clínicas seriadas, por dois oftalmologistas especialistas em córnea, através das fotografias, de forma cegada e randomizada para as variáveis extensão dos vasos e grau de inflamação/calibre dos vasos. As avaliações foram comparadas utilizando a estatística de Kappa para comprovar a reprodutibilidade do método.
1º) Extensão dos vasos determinada em escala de 0 a 4, a saber:
Grau 0 - sem vasos no limbo corneano.
Grau 1 - vasos que avançam sobre o limbo corneano, chegando até ¼ da área queimada.
Grau 2 - vasos que chegam até ½ da área queimada.
Grau 3 - vasos que chegam até ¾ da área queimada.
Grau 4 - vasos que se estendem por toda a área queimada.
2º) Grau de inflamação e calibre dos vasos foram determinados em escala de 0 a 3, a saber:
Grau 0 - sem inflamação ou vasos.
Grau 1 - pouca inflamação, vasos de pequeno calibre.
Grau 2 - reação inflamatória moderada, vasos de médio calibre.
Grau 3 - reação inflamatória intensa, vasos de grande calibre.
Logo após a realização das fotografias, os animais foram sacrificados com dose de 5 ml de pentobarbital sódico intramuscular.
Em seguida, foi realizada a extração da córnea direita de todos os animais, sendo mantida margem escleral de 3 mm. Após a retirada, as córneas foram fixadas por 24 horas em formalina e preparadas para o estudo histopatológico.
Foram realizados cortes longitudinais, incluindo toda a córnea, sendo as alterações encontradas coincidentes com a área aonde foi realizada a queimadura. A espessura do corte foi de 3 micra, a parafina foi removida e o tecido reidratado, para poder sofrer coloração com hematoxilina-eosina.
Foi sempre computada para a avaliação a lâmina com maior dano. Foi observado o estado epitelial com o auxilio do microscópio, classificando as córneas em duas categorias: epitélio íntegro e epitélio erosado.
A análise quantitativa do número de polimorfonucleares por campo de grande aumento foi realizada utilizando um aumento de 400 vezes em um microscópio ótico Nikon® (Nikon Inc. Melville - Estados Unidos da América) modelo eclipse E200.
A reprodutibilidade do modelo de avaliação (análise fotográfica) utilizado foi validado considerando a estatística de Kappa.
Em cada um dos momentos de avaliação, os dois grupos foram comparados em relação a variáveis ordinais (extensão dos vasos e inflamação/calibre dos vasos) considerando-se o teste não-paramétrico de Mann-Whitney. Já a comparação dos grupos dentro de cada momento para variáveis dicotômicas (epitélio integro ou erosado), foi efetuada considerando-se o teste exato de Fisher. Valores de p<0,05 indicaram significância estatística.
RESULTADOS
No dia 18 após a queimadura química da córnea, 2 coelhos do grupo controle morreram e foram excluídos da pesquisa. Desta forma, permaneceram no estudo 18 animais, sendo 8 do grupo controle e 10 do grupo de estudo.
ANÁLISE FOTOGRÁFICA
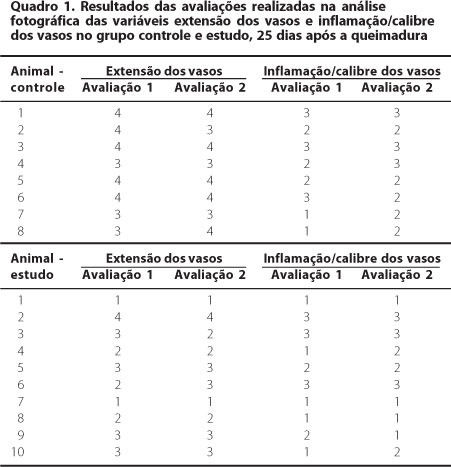
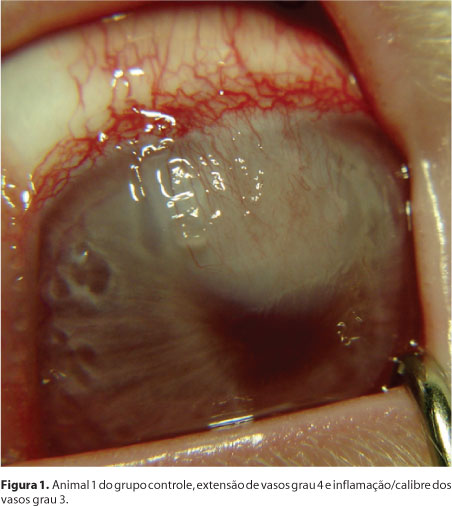
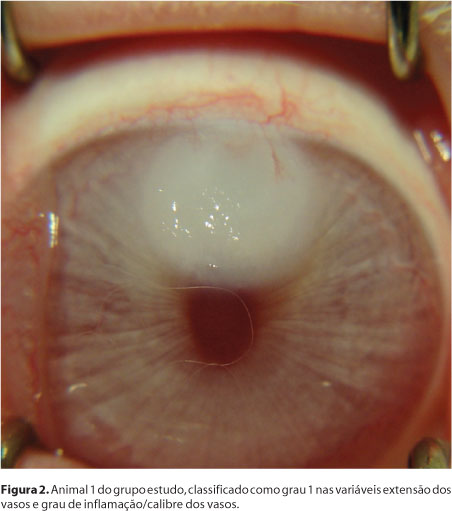
As variáveis estudadas foram extensão dos vasos e grau de inflamação/calibre dos vasos. As fotografias digitais de cada animal foram submetidas a duas avaliações de cada variável (Quadro 1). Na figura 1, observa-se o animal 1 do grupo controle. Em contraste, o animal 1 do grupo estudo (Figura 2).
ANÁLISE DE CONCORDÂNCIA
- Variável extensão dos vasos: Para a variável extensão dos vasos a estimativa do coeficiente de Kappa foi igual 0,705 (Intervalo de Confiança de 95%: 0,514 - 0,895) indicando um bom grau de concordância entre as duas avaliações. A concordância fica melhor caracterizada nos graus mais extremos: grau 1, apresenta coeficiente de Kappa de 0,863 (IC 95% de 0,541 - 1) e grau 4, com coeficiente de Kappa de 0,824 (IC 95% 0,502 - 1).
- Variável Grau de inflamação/Calibre dos vasos: a estimativa do coeficiente de Kappa foi igual a 0,500 (intervalo de confiança entre 0,269 e 0,731) indicando um bom grau de concordância entre as duas avaliações. A concordância apresenta-se fraca nos graus 1 e 2, apresentando coeficiente de Kappa 0,383 (IC 95% 0,061 - 0,706) e 0,339 (IC 95% 0,017 - 0,661), respectivamente, indicando certo grau de dúvida em vasos de calibre pequeno ou médio, havendo uma boa reprodutibilidade das avaliações em vasos de grande calibre (grau 3), apresentando coeficiente de Kappa 0,853 (IC 95% 0,531 - 1) (Tabela 1).
COMPARAÇÃO ENTRE GRUPOS
Nas análises subsequentes foi considerada a média das duas avaliações.
VARIÁVEIS EXTENSÃO DOS VASOS E INFLAMAÇÃO/CALIBRE DOS VASOS
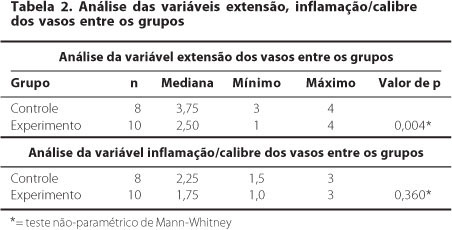
Vinte e cinco dias após a queimadura química, o grupo estudo apresentou uma extensão dos vasos significativamente menor que o grupo controle.
Em relação à inflamação/calibre dos vasos, apesar de encontrarmos valores menores no grupo estudo, a diferença não foi significativa (Tabela 2).
ANÁLISE HISTOPATOLÓGICA
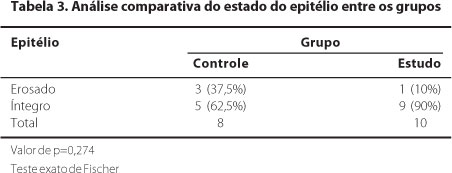
Com relação ao estado do epitélio, somente um coelho do grupo estudo apresentou epitélio erosado (10%). No grupo controle, 3 coelhos apresentaram erosão do epitélio (37,5%), não havendo diferença estatisticamente significativa (Tabela 3).
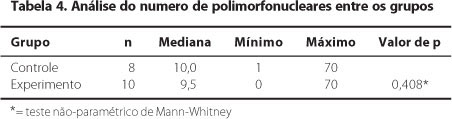
Foi realizada uma avaliação histológica quantitativa em relação ao número de polimorfonucleares encontrados por campo de grande aumento, não sendo encontrado diferença significativa entre os grupos estudo e controle (Tabela 4).
DISCUSSÃO
Neste trabalho procurou-se avaliar o efeito do bevacizumabe em modelo experimental de córnea de coelho. Para a investigação de uma substância antiangiogênica necessita-se de um modelo que permita acessibilidade, visibilidade e acompanhamento temporal do crescimento dos vasos sanguíneos. O coelho foi escolhido por apresentar estas características(17-19).
De acordo com a análise estatística realizada com os dados obtidos da pesquisa confirmou-se que o método utilizado reproduziu adequadamente o que ocorreu com os vasos. Estes resultados obtidos mostraram que o método utilizado pode ser reproduzido para avaliação de outras drogas antiangiogênicas na córnea.
A diminuição da extensão dos vasos comprova o efeito esperado da droga nas queimaduras químicas e está de acordo com os dados encontrados na literatura recente(20-21). Os estudos também mostram que o efeito da droga é maior se esta é aplicada simultaneamente com a cauterização química. Considerando que a presença de neovasos é um fator conhecido de mau prognóstico em transplante de córnea, além de interferir na transparência corneana e causar baixa acuidade visual(1), a droga tem potencial para melhora de prognóstico em casos de queimadura química, principalmente naqueles casos em que seria realizado um transplante de córnea em um momento posterior.
O grau de inflamação foi avaliado visto que existem estudos que, apesar da droga não apresentar efeitos anti-inflamatórios diretos, mostram evidencias de um efeito em fibroblastos(21-22). A ação na inflamação aguda ainda não havia sido estudada mais profundamente, sendo sugerido uma diminuição na invasão de neutrófilos na ferida(23). Os resultados mostraram que a droga não tem um efeito anti-inflamatório clinicamente significativo. Isso corrobora que a inflamação possui varias vias e que a inibição da via do VEGF não possibilita um controle adequado da inflamação.
O estudo histopatológico do número de polimorfonucleares mostrou um número menor dessas células inflamatórias nas córneas do grupo estudo comparado ao grupo controle. Entretanto, os números não obtiveram significância estatística, indo de acordo com os dados anteriormente citados de que o efeito direto da droga na inflamação aguda não é significativo. Os efeitos sobre a inflamação aguda podem ocorrer devido à diminuição do aporte sanguíneo e consequentemente a uma maior dificuldade para as células inflamatórias chegarem ao local da inflamação e não por um efeito direto da droga nos mecanismos celulares como ocorre com o corticóide.
A associação do bevacizumabe com corticóide mostrou em estudo recente(24) não ter efeito sinérgico ou aditivo em relação a inibição da neovascularização corneana. Entretanto, a modulação dos efeitos deletérios do processo inflamatório intenso com essa associação não foi avaliada. São necessários mais estudos para estabelecer a segurança desta associação, pois a inibição intensa da inflamação e da neovascularização combinadas podem levar a um quadro teórico de morte celular por hipóxia aguda, devido à inibição de todos os mecanismos fisiológicos envolvidos em um quadro isquêmico desta natureza(25).
A opacidade resultante da queimadura química não foi avaliada no presente estudo. O efeito do bevacizumabe foi avaliado na literatura recente(21), que mostrou não haver alteração significativa no grau de opacidade final. O estudo da associação do bevacizumabe com drogas como corticóides ou ciclosporina, drogas com efeito direto que comprovadamente reduzem a opacidade corneana após a queimadura(26), é promissor.
O estado do epitélio corneano foi avaliado, pois a droga tem o potencial de alterar a cicatrização, tendo sido descrito o atraso na cicatrização de feridas (Avastin®). O epitélio íntegro é fundamental no processo cicatricial, diminuindo a possibilidade de contaminação secundária da ferida, sendo o atraso na re-epitelização um fator negativo para o seu uso em lesões oculares. A comparação entre os dois grupos não mostrou um atraso na re-epitelização do grupo estudo, sugerindo segurança da droga em situações de defeito epitelial. Trabalhos recentes mostram um atraso no fechamento epitelial(27) contrastando com o resultado encontrado no presente estudo. Entretanto, o tratamento foi realizado com bevacizumabe tópico várias vezes ao dia, no qual a droga tem um contato direto com o epitélio corneano; enquanto no presente trabalho foi realizado aplicação subconjuntival, em que a droga não atinge as células epiteliais diretamente. Supõe-se então que esta seja a via mais segura, visto que neste estudo não prejudicou a re-epitelização. Estudo utilizando bevacizumabe subconjuntival com análise de re-epitelização em ratos(28) também mostrou que a droga tem o potencial de acelerar a regeneração da membrana basal, podendo ter efeito benéfico no fechamento da ferida (em contraste com o atraso na re-epitelização causado por corticóides).
A neovascularização induzida pela queimadura foi suprimida, porém não totalmente. Isso se deve possivelmente ao VEGF não ser a única via angiogênica e mesmo como tratamento, outros fatores pró-angiogênicos continuam agindo como TGF-Beta e o fator de crescimento de fibroblasto(19). Sugere-se que o bevacizumabe não deve ser utilizado como monoterapia e pode ser parte do tratamento para quadros agudos agindo em conjunto com outras drogas como corticóides.
Estudos com outros quadros devidos a neovasos antigos como a retinopatia diabética(19,29) mostram uma recidiva importante dos vasos após a supressão do medicamento, devendo o tratamento ser realizado seguidamente. Para quadros agudos de neovascularização como queimaduras ou início de neovascularização após um transplante de córnea, o efeito da droga ainda não foi extensivamente estudado e é possível que se diminuirmos o estímulo angiogênico na fase aguda, com o uso de inibidores específicos como o bevacizumabe, podemos ter uma diminuição dos neovasos a longo prazo, já que nesses casos o estímulo angiogênico é de curta duração e não parte da fisiopatologia da doença como na retinopatia diabética. Esse tratamento seria então muito benéfico a longo prazo, podendo inclusive facilitar tratamentos como um transplante de córnea em um momento posterior.
O bevacizumabe tem potencial para uso em casos graves que geralmente apresentam prognóstico reservado e sem tratamentos eficazes atualmente disponíveis. Várias linhas de pesquisa sobre a droga podem ser exploradas utilizando doses, vias de administração e períodos diferentes, com ênfase em um prazo mais longo.
CONCLUSÕES
O modelo experimental é adequado e pode ser reproduzido e utilizado para avaliar outras drogas antiangiogênicas na córnea.
O estudo revelou que há uma diferença estatisticamente significativa em relação à extensão dos vasos, sendo menor no grupo de estudo. Não houve diferença significativa entre os grupos em relação à inflamação ou calibre dos vasos, tanto pela análise fotográfica como para estudo histopatológico. A droga não atrasou a re-epitelização da córnea após a queimadura.
AGRADECIMENTOS
Ao professor Dr. Oswaldo Malafaia, coordenador do Programa de Pós-Graduação em Princípios de Cirurgia do Hospital Universitário Evangélico de Curitiba e da Faculdade Evangélica do Paraná, pela oportunidade de desenvolvimento da pesquisa no Instituto de Pesquisas Médicas (IPEM).
REFERÊNCIAS
1. Chang JH, Gabison EE, Kato T, Azar DT. Corneal neovascularization. Curr Opin Ophthalmol. 2001;12(4):242-9.
2. Lee P, Wang CC, Adamis AP. Ocular neovascularization: an epidemiologic review. Surv Ophthalmol. 1998;43(3):245-69.
3. Koay PY, Lee WH, Figueiredo FC. Opinions on risk factors and management of corneal graft rejection in the United Kingdom. Cornea. 2005;24(3):292-6.
4. Kuckelkorn R, Schrage N, Keller G, Redbrake C. Emergency treatment of chemical and thermal eye burns. Acta Ophthalmol Scand. 2002;80(1):4-10. Review.
5. Kvanta A. Ocular angiogenesis: the role of growth factors. Acta Ophthalmol Scand. 2006; 84(3):282-8.
6. Benelli U, Bocci G, Danesi R, Lepri A, Bernardini N, Bianchi F, et al. The heparan sulfate suleparoide inhibits rat corneal angiogenesis and in vitro neovascularization. Exp Eye Res. 1998;67(2):133-42.
7. Papathanassiou M, Theodossiadis PG, Liarakos VS, Rouvas A, Giamarellos-Bourboulis EJ, Vergados IA. Inhibition of corneal neovascularization by subconjunctival bevacizumab in an animal model. Am J Ophthalmol. 2008;145(3):424-31.
8. Philipp W, Speicher L, Humpel C. Expression of vascular endothelial growth factor and its receptors in inflamed and vascularized human corneas. Invest Ophthalmol Vis Sci. 2000; 41(9):2514-22.
9. Gan L, Fagerholm P, Palmblad J. Vascular endothelial growth factor (VEGF) and its receptor VEGFR-2 in the regulation of corneal neovascularization and wound healing. Acta Ophthalmol Scand. 2004;82(5):557-63.
10. Adamis AP, Miller JW, Bernal MT, D'Amico DJ, Folkman J, Yeo TK, Yeo KT. Increased vascular endothelial growth factor levels in the vitreous of eyes with proliferative diabetic retinopathy. Am J Ophthalmol. 1994;118(4):445-50.
11. Tripathi RC, Li J, Tripathi BJ, Chalam KV, Adamis AP. Increased level of vascular endothelial growth factor in aqueous humor of patients with neovascular glaucoma. Ophthalmology. 1998;105(2):232-7.
12. Kvanta A, Algvere PV, Berglin L, Seregard S. Subfoveal fibrovascular membranes in age-related macular degeneration express vascular endothelial growth factor. Invest Ophthalmol Vis Sci. 1996;37(9):1929-34.
13. Manzano RP, Peyman GA, Khan P, Kivilcim M. Testing intravitreal toxicity of bevacizumab (Avastin). Retina. 2006;26(3):257-61.
14. Kahook ML, Lin SC. Anti-VEGF therapy: next stop glaucoma? Curr Ophthalmol. 2008;15(5):47-9.
15. Gehlen ML, Moreira H, Moreira L, Sabag FP, Repka JCD. Avaliação espectrofotométrica do azul de Evans na reação inflamatória da córnea: estudo experimental em coelhos. Arq Bras Oftalmol. 2004;67(2):219-25.
16. Fechine-Jamacaru FV. Modelo de angiogênese inflamatória em córnea de coelho induzida pela cauterização alcalina pontual. Acta Cir Bras. 2005;20(1):64-73.
17. D'Amato RJ, Loughnan MS, Flynn E, Folkman J. Thalidomide is an inhibitor of angiogenesis. Proc Natl Acad Sci U S A. 1994;91(9):4082-5.
18. Auerbach R, Lewis R, Shinners B, Kubai L, Akhtar N. Angiogenesis assays: a critical overview. Clin Chem. 2003;49(1):32-40.
19. Yoeruek E, Ziemssen F, Henke-Fahle S, Tatar O, Tura A, Grisanti S, Bartz-Schmidt KU, Szurman P; Tübingen Bevacizumab Study Group. Safety, penetration and efficacy of topically applied bevacizumab: evaluation of eyedrops in corneal neovascularization after chemical burn. Acta Ophthalmol. 2008;86(3):322-8.
20. Hosseini H, Nejabat M, Mehryar M, Yazdchi T, Sedaghat A, Noori F. Bevacizumab inhibits corneal neovascularization in an alkali burn induced model of corneal angiogenesis. Clin Experiment Ophthalmol. 2007;35(8):745-8.
21. Hurmeric V, Mumcuoglu T, Erdurman C, Kurt B, Dagli O, Durukan AH. Effect of subconjunctival bevacizumab (Avastin) on experimental corneal neovascularization in guinea pigs. Cornea. 2008;27(3):357-62.
22. Li Z, Van Bergen T, Van de Veire S, Van de Vel I, Moreau H, Dewerchin M, et al. Inhibition of vascular endothelial growth factor reduces scar formation after glaucoma filtration surgery. Invest Ophthalmol Vis Sci. 2009;50(11):5217-25.
23. Saravia M, Zapata G, Ferraiolo P, Racca L, Berra A. Anti-VEGF monoclonal antibody-induced regression of corneal neovascularization and inflammation in a rabbit model of herpetic stromal keratitis. Graefes Arch Clin Exp Ophthalmol. 2009;247(10):1409-16.
24. Kang S, Chung SK. The effect of subconjuctival combined treatment of bevacizumab and triamcinolone acetonide on corneal neovascularization in rabbits. Cornea. 2010;29(2):192-6.
25. Donshik PC, Berman MB, Dohlman CH, Gage J, Rose J. Effect of topical corticosteroids on ulceration in alkali-burned corneas. Arch Ophthalmol. 1978;96(11):2117-20
26. Den S, Sotozono C, Kinoshita S, Ikeda T. Efficacy of early systemic betamethasone or cyclosporin A after corneal alkali injury via inflammatory cytokine reduction. Acta Ophthalmol Scand. 2004;82(2):195-9.
27. Kim TI, Chung JL, Hong JP, Min K, Seo KY, Kim EK. Bevacizumab application delays epithelial healing in rabbit cornea. Invest Ophthalmol Vis Sci. 2009;50(10):4653-9.
28. Lee SH, Leem HS, Jeong SM, Lee K. Bevacizumab accelerates corneal wound healing by inhibiting TGF-beta2 expression in alkali-burned mouse cornea. BMB Rep. 2009;42(12):800-5.
29. Brown DM, Regillo CD. Anti-VEGF agents in the treatment of neovascular age-related macular degeneration: applying clinical trial results to the treatment of everyday patients. Am J Ophthalmol. 2007;144(4):627-37.
Endereço para correspondência:
Glauco Reggiani Mello
668 - Euclid Avenue Unit 506
Zip 44114 Cleveland, OH USA
E-mail: [email protected]
Recebido para publicação em 04.07.2010
Última versão recebida em 30.10.2010
Aprovação em 21.11.2010
Trabalho realizado no Programa de Pós-Graduação em Princípios de Cirurgia do Hospital Universitário Evangélico de Curitiba e da Faculdade Evangélica do Paraná - Curitiba (PR), Brasil.
Nota Editorial: Depois de concluída a análise do artigo sob sigilo editorial e com a anuência do Dr. Vinícius Coral Ghanem e Procópio Miguel dos Santos sobre a divulgação de seu nome como revisor, agradecemos sua participação neste processo.
How to cite this article: