
Alan Diego Negretto1; André Marcelo Vieira Gomes2; Fernando Pistarini Gonçalves3; Huang Sheau Jiun4; Suel Abujamra5; Yoshitaka Nakashima7
DOI: 10.1590/S0004-27492007000500010
RESUMO
OBJETIVO: Avaliar a anatomia do buraco macular idiopático (BMI) a partir da tomografia de coerência óptica (OCT) e construir índice prognóstico que possa ser correlacionado com os resultados visuais e o fechamento anatômico. MÉTODOS: Estudo prospectivo, no qual 22 olhos com BMI foram avaliados pelo OCT no pré-operatório da cirurgia do BMI. Foi criado o índice prognóstico do buraco macular (IPBM) que foi correlacionado com o resultado anatômico e a acuidade visual pós-operatória seis meses após a cirurgia. RESULTADOS: Dezesseis olhos (72,7%) obtiveram fechamento anatômico ao final de seis meses de acompanhamento. Na análise do IPBM, houve diferença significativa entre o grupo 1 (BM aberto) e o grupo 2 (BM fechado) (p=0,0018). O risco de insucesso para o fechamento anatômico é 11 vezes maior quando o diâmetro da base interna for superior a 600 µm ou o IPBM for inferior a 0,6 (p=0,0495). No que diz respeito à AV final, observou-se que o IPBM tem correlação negativa significante na AV (p=0,001). CONCLUSÃO: O IPBM se apresentou como o melhor preditor de fechamento anatômico e acuidade visual pós-operatória entre as variáveis aqui estudadas. Responde por 41% da acuidade visual pós-operatória final, nos levando a crer que outros fatores, como o tempo de história e a degeneração dos fotorreceptores nestes BM mais antigos, possam estar envolvidos nos resultados visuais.
Descritores: Macula lutea; Macula lutea; Tomografia de coerência óptica; Acuidade visual; Vitrectomia
ABSTRACT
PURPOSE: To evaluate the anatomy of idiopathic macular hole (IMH) using Optical Coherence Tomography (OCT) and to construct a prognostic index that can be correlated with the visual outcomes and the anatomical closing. METHODS: Prospective study, in which 22 eyes with IMH had been evaluated through OCT in the daily postoperative period of IMH surgery. The Prognostic of Macular Hole Index (PMHI) was created which was correlated with the anatomical result and the postoperative visual acuity (VA) six months after surgery. RESULTS: Sixteen eyes (72.7%) got anatomical closing at the end of six months of follow-up. On analysis of PMHI, there was significant difference between group 1 (open MH) and group 2 (closed MH) (p=0.0018). The risk for failure of anatomical closing is 11 times greater when the diameter of the internal base is over 600 µm or IPBM is less than 0.6 (p=0.0495). Regarding final VA, it was observed that the IPBM had a significant negative correlation with AV (p=0.001). CONCLUSIONS: IPBM showed to be the best predictor of anatomical closing and postoperative visual acuity among the studied variables. It predicted 41% of the postoperative final visual acuity, leading us to believe that other factors, such as the time of history and the degeneration of photoreceptors in these older BM, can be involved in the visual outcomes.
Keywords: Macular lutea; Macula lutea; Tomography, optical coherence; Visual acuity; Vitrectomy
INTRODUÇÃO
O buraco macular idiopático (BMI) é um defeito retiniano de gênese controversa envolvendo primariamente a fovéola. Afeta principalmente as mulheres (67 a 91%) entre a quinta e sétima décadas de vida, sendo bilaterais em torno de 3 a 27% dos casos(1-2).
Um grande impulso no tratamento do BMI foi proporcionado pelas observações iniciais de Gass(3), pelo desenvolvimento da técnica cirúrgica por Kelly e Wendel(4) e finalmente, pela inclusão do tomografia de coerência óptica (OCT) no arsenal diagnóstico da oftalmologia(5).
A vitrectomia com a remoção ou não da membrana limitante interna (MLI) tornou-se uma técnica mundialmente aceita e têm melhorado significativamente as taxas de fechamento do BMI(6).
Atualmente consegue-se sucesso anatômico entre 80 e 90% com melhora da acuidade visual em 55 a 85% dos casos(7).
Diversos autores comprovaram que entre 25 a 50% dos BMI fechados não conseguem acuidades visuais melhores que 20/50(8-9).
Percebe-se, portanto, que um substancial número de pacientes não apresentam melhora visual apesar do sucesso anatômico de suas cirurgias.
Mesmo assim, a cirurgia mostra-se benéfica na melhora do escotoma central e na qualidade de vida destes pacientes(10).
Nos últimos anos, vários fatores têm sido pesquisados no intuito de correlacioná-los com os resultados visuais obtidos após a cirurgia do BMI.
A acuidade visual pré-operatória, o tamanho do BMI(11-12) e a duração dos sintomas(13) têm sido objetos de estudo durante muito tempo.
Outros testes mais sofisticados como a medida da acuidade visual potencial (PAM)(14), quantidade do fluido sub-retiniano ao OCT(15), interferometria a laser(14), eletrorretinograma macular focal(16) também foram propostos com algum grau de sucesso.
Alguns pesquisadores, avaliaram medidas anatômicas do BMI na criação de índices prognósticos relacionando-os com a acuidade visual final(17-18).
Contudo ainda hoje, pequena atenção se dá à anatomia pré-operatória do buraco. A cirurgia do BMI é cercada de certa imprevisibilidade quanto ao fechamento anatômico e seus resultados visuais. Somente com a análise dos fatores pré-operatórios já conhecidos, a tarefa do cirurgião quanto à orientação de seus pacientes em relação ao prognóstico da cirurgia fica dificultada.
O objetivo deste estudo é avaliar a correlação das medidas anatômicas isoladas (altura, base externa, base interna) do BMI obtidas a partir do OCT e construir, se possível, um índice prognóstico que possa ser correlacionado com os resultados visuais e o fechamento anatômico.
MÉTODOS
Pacientes
Estudo clínico prospectivo, realizado em conjunto no Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo - (FMUSP) e no Instituto Suel Abujamra, São Paulo-SP, entre 2006 e 2007, no qual 22 olhos com BMI de 22 pacientes foram avaliados segundo as medidas apresentadas ao exame de OCT (Stratus OCTIII, Carl Zeiss, Dublin, CA) no pré-operatório.
Outras variáveis incluíram sexo, idade, etnia, estágio do BM pela classificação biomicroscópica de Gass, tempo do aparecimento da doença informado pelo paciente (<6 meses, 6 meses - 1 ano, >1 ano), acuidade visual pré e pós-operatória utilizando o logaritmo de mínimo ângulo de resolução (logMAR) e o resultado anatômico da mácula após a cirurgia.
Pacientes com história de trauma, catarata, miopia maior que 6 dioptrias, vitrectomia prévia para BM ou não, presença de membrana epirretiniana (MER) associada e outras opacidades de meios foram excluídos do estudo.
Tomografia de coerência óptica (OCT)
Após o consentimento livre e esclarecido, os pacientes foram submetidos ao exame de OCT. O mesmo examinador experiente com certificação em centros de leitura como de Visconsin (USA) e Viena (Áustria) realizou 3 medidas utilizando o corte "Cross-Hair" de 5 mm disposto no centro do buraco. Para manter a boa confiabilidade das medidas, optou-se pela realização dos "scans" com intervalo de 5 minutos entre eles.
As medidas foram realizadas com o auxílio do compasso do OCT e optou-se pela eliminação da opção que identifica a espessura da camada de fibras nervosas utilizada pelo software do aparelho em virtude de estudos já apontarem diferenças significativas entre os dois métodos(19).
A escolha da imagem utilizada para definir as medidas isoladas (altura, base interna, base externa), foi definida seguindo os critérios (Figura 1):
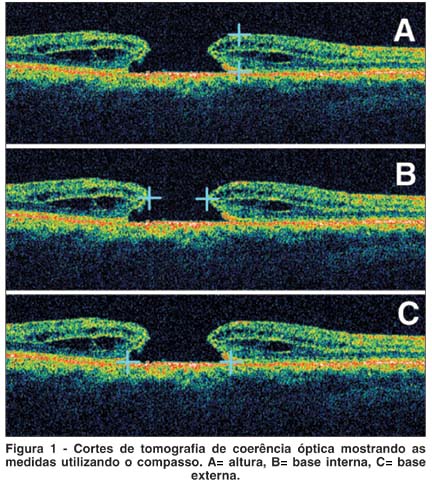
imagem de melhor qualidade, que permita a completa visualização das bordas do BMI.
maior diâmetro interno do buraco indiferente do eixo (90º ou 180º) medido em µm.
maior diâmetro externo do buraco obtido ao nível do epitélio pigmentado da retina (EPR), indiferente do eixo (90º ou 180º), medido em µm.
maior altura obtida a partir do EPR até o bordo do BM medido em µm.
Com as medidas isoladas foi possível calcular (Figura 2): Índice prognóstico do buraco macular (IPBM) - obtido pela divisão da altura dos bordos pelo diâmetro da base interna do BM.
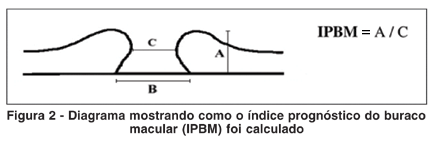
As medidas isoladas (altura, base interna e base externa) juntamente com o IPBM foram correlacionadas com o fechamento anatômico e a AV logMAR corrigida.
Para manter a fidedignidade das medidas, o comprimento axial de todos os olhos foi medido através de biometria A-Scan.
Técnica cirúrgica
A técnica cirúrgica empregada foi a vitrectomia posterior via pars plana, 20 gauge, padrão três "portas" com retirada da MLI através de microfórceps sem utilização de corantes e injeção intravítrea de C3F8 a 14% ao final do procedimento por um único cirurgião experiente.
O estágio do BMI era confirmado intra-operatoriamente, assim como o descolamento do vítreo posterior (DVP) e presença ou não de MER.
O descolamento da hialóide posterior foi confirmado pelo anel de Weiss e o restante do vítreo foi ressecado além das arcadas vasculares.
No BM estágio 4, atenção foi dada à remoção da hialóide posterior devido à possibilidade de ocorrência de vitreosquise.
No final da cirurgia, a periferia retiniana foi cuidadosamente examinada a fim de se identificar e tratar roturas periféricas.
Os pacientes foram orientados quanto ao posicionamento do olhar para baixo durante sete dias após a cirurgia. O acompanhamento pós-operatório seguiu-se no primeiro e sétimo dia, duas semanas, um, três e seis meses.
Foi considerado sucesso anatômico a ausência do defeito retiniano com resolução de cisto ou fluido sub-retiniano. A morfologia foveal pós-operatória não foi objeto de estudo.
Análise estatística
As variáveis classificatórias foram descritivamente apresentadas em tabelas de contingência contendo freqüências absolutas (n) e relativas (%). A associação entre elas e as variáveis resposta (fechada e aberta) foram avaliadas com o teste da razão de verossimilhança ou teste exato de Fisher.
As variáveis quantitativas foram apresentadas descritivamente em tabelas contendo média e desvio padrão. As médias foram comparadas com o teste t-Student.
As variáveis que apresentaram significância estatística na análise univariada, foram utilizadas no ajuste do modelo de regressão logística.
Foram calculadas coeficientes de correlação de Pearson entre as variáveis quantitativas e a variável AV pós. As variáveis foram utilizadas no modelo de regressão linear com procedimento "stepwise" de seleção de variáveis.
Os valores de p<0,05 foram considerados estatisticamente significantes.
RESULTADOS
Os pacientes estudados apresentavam idades entre 45 a 77 anos de idade, com média de 65,73 anos e desvio padrão de 8,82 anos. Dezessete (77,3%) foram do sexo feminino (77,3%), sendo dezoito (81,8%) brancos e 4 (18,2%) negros.
Quanto ao tempo do aparecimento dos sintomas relatado pelos pacientes, em 4 (18,2%) foi menor que 6 meses, em 5 (22,7%) de 6 meses a 1 ano, e em 13 (59,1%) maior que 1 ano.
Com base na classificação biomicroscópica de Gass, os BM foram divididos em: 1 (4,5%) estágio II, 8 (36,4%) estágio III e 13 (59,1%) estágio IV.
A AV logMAR medida no pré-operatório, oscilou entre 0,60 (20/80) e 1,60 (20/800), com média de 1,09 (20/200). No sexto mês de pós-operatório, a AV variou entre 0,0 (20/20) e 1,60 (20/800) com média de 0,69 (20/100). A média de melhora da AV após a cirurgia foi de 4,09 linhas.
O tempo de seguimento dos pacientes variou de 6 a 19 meses com média de 10,45 meses (Tabela 1).
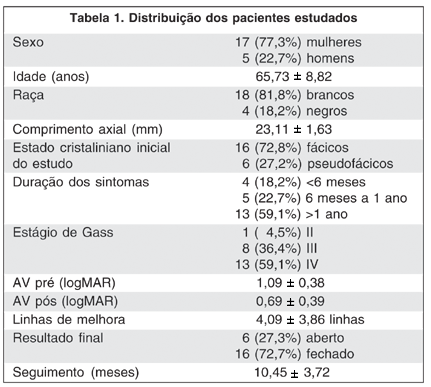
As medidas anatômicas dos BM as dimensões estudadas variaram da seguinte forma:
maior diâmetro da base externa (BE): entre 442 e 2051 µm, com média de 1090,32 µm e desvio padrão de 340,16 µm;
maior diâmetro da base interna (BI): entre 237 e 1172 µm, com média de 602,68 µm e desvio padrão de 251,74 µm;
maior altura dos bordos (A): entre 290 e 730 µm, com média de 413,05 µm desvio padrão de 91,96 µm;
IPBM entre 0,364 e 1,679, com média de 0,818 e desvio padrão de 0,411;
Após a vitrectomia obteve-se o fechamento anatômico do BM em 16 olhos (72,7%).
Antes do procedimento cirúrgico, 6 olhos (27,2%) eram pseudofácicos e 16 olhos (72,8%) eram fácicos. Houve o desenvolvimento de catarata em 11 (68,7%) destes olhos dentro dos primeiros seis meses após a vitrectomia e foram submetidos à facoemulsificação com implante de lente intra-ocular, sem intercorrências.
Nenhum dos olhos teve vitreosquise identificada no momento da cirurgia.
Quatro olhos (18,1%) tiveram pequenas roturas periféricas identificadas durante a vitrectomia necessitando tratamento com fotocoagulação a laser no intra-operatório.
Nenhum dos pacientes apresentou quadro de descolamento de retina (DR) após a cirurgia em todo o período de seguimento.
Fechamento anatômico
Na primeira análise, cada variável foi independentemente relacionada com o fechamento anatômico do BMI (Tabela 2).
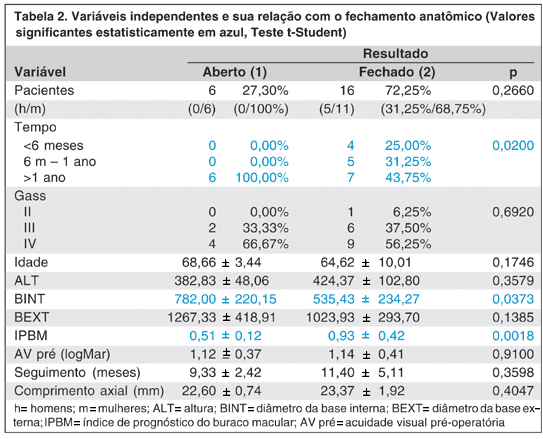
Não houve diferenças significativas em relação à distribuição de sexo, idade, AV pré, comprimento axial e tempo de seguimento entre os pacientes dos grupos 1 (BM aberto) e 2 (BM fechado).
Em todos os pacientes com BM aberto, o tempo de duração dos sintomas foi superior a 1 ano quando comparados aos pacientes com BM fechado (43,75%).
Não foi observada associação entre a classificação biomicroscópica de Gass e o fechamento anatômico do BMI.
Em relação às medidas anatômicas isoladas, a altura (ALT) e o diâmetro da base externa (BEXT), não houve diferenças entre os grupos estudados.
O diâmetro da base interna (BINT) teve uma média estatisticamente superior no grupo 1 (782,00 µm) em relação às médias do grupo 2 (535,43 µm), Teste t-Student, p=0,373.
Na análise do índice IPBM, houve diferença significativa entre o grupo 1 (0,51) e o grupo 2 (0,93) para a amostra estudada (n=22).
Como era de se esperar, a acuidade visual pós-operatória (logMAR) foi superior no grupo 2 em relação ao grupo 1 (p=0,002)
Na análise multivariada entre as variáveis significantes no teste t-Student (tempo, diâmetro da base interna e IPBM) o índice IPBM foi a variável selecionada. Através de uma curva ROC obteve-se valores de corte de <600 µm e >600 µm para o BINT e <0,6 e >0,6 para o IPBM.
A análise de regressão logística apontou que se o diâmetro da base interna for superior a 600 µm ou o IPBM for inferior a 0,6, tem-se um risco 11 vezes maior de insucesso no fechamento anatômico do BMI (Odds Ratio= 11,000, p=0,0495).
Acuidade visual final
Em outra análise, as mesmas variáveis independentes foram submetidas ao teste de correlação de Pearson para verificar sua relação com a AV corrigida logMAR medida no sexto mês após a cirurgia (Tabela 3).
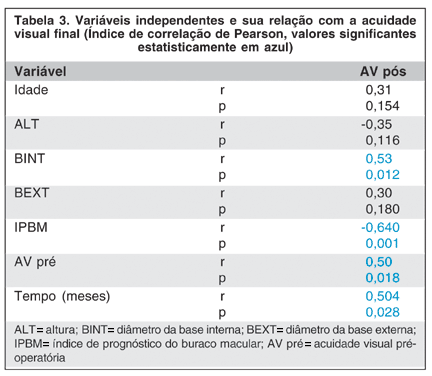
Observou-se, que as variáveis BINT, AV pré e tempo (meses) têm uma correlação positiva significante na AV final, ou seja, quanto maior o valor destas variáveis maior a AV na escala logMAR. Vale lembrar que na escala logMAR quanto maior o valor, pior é a AV na escala de Snellen (1,0 = 20/200).
Por outro lado, a variável IPBM tem uma correlação negativa significante na AV final, ou seja, quanto maior o valor desta variável menor a AV na escala logMAR (melhor visão).
A regressão linear entre as variáveis significantes (BINT, IPBM, AV pré e IBPM) a variável IPBM foi selecionada (p=0,0013). O modelo aponta que dentre estas variáveis, o IBPM responde sozinho por 41% da AV pós-operatória.
O gráfico 1 ilustra que à medida que o valor do índice IPBM aumenta, a acuidade visual melhora.
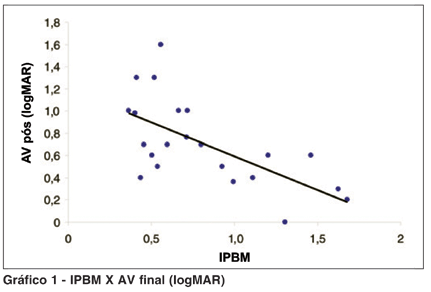
DISCUSSÃO
O principal achado em nosso estudo foi de que a anatomia pré-operatória do buraco macular idiopático analisada por meio de tomografia de coerência óptica pode trazer várias informações de grande utilidade ao cirurgião de vítreo-retina.
Kelly e Wendel(4) foram os primeiros a buscar fatores prognósticos na cirurgia do BMI. Observaram que a duração dos sintomas inferior a seis meses era um importante fator prognóstico na melhora da AV final.
Alguns autores fizeram ressalva quanto ao limitado prognóstico cirúrgico de BMI superiores há um ano, alegando que o processo degenerativo dos fotorreceptores seria um limitador na melhoria da AV(20).
Em nossa análise, todos os pacientes (100%) com BM que não fecharam tinham sintomas há mais de um ano quando comparados com os pacientes com BM fechado (43,75%).
Ainda com relação ao tamanho do BM, foi observado que BMIs de pequeno diâmetro eram associados com melhores resultados visuais. A razão para isso poderia ser a maior preservação da mácula nos buracos menores(21).
O diâmetro externo que não pode ser visualizado pela lâmpada de fenda e sim apenas com o auxílio do OCT, não se mostrou com melhor correlação na AV e fechamento que o diâmetro interno.
Alguns pesquisadores analisaram a influência do tamanho do BMI na AV final de 94 pacientes. Identificaram uma correlação negativa significativa entre os diâmetros interno e externo com a AV. Notaram também, que nos casos em que os BMI permaneceram abertos após o primeiro procedimento, seus diâmetros (interno e externo) eram significativamente maiores quando comparados àqueles BMI fechados cirurgicamente(13).
Em nossa série, observamos que a BEXT não difere entre os grupos estudados. Porém, o diâmetro da BINT teve uma média estatisticamente superior no grupo de BM aberto (782,00 µm) em relação às médias do grupo BM fechado (535,43 µm)
A primeira geração de OCTs foi utilizada na criação de índices prognósticos na cirurgia do BMI.
Alguns autores empregaram a razão entre a soma das alturas da borda esquerda e direita pela base interna do buraco foi utilizada na criação de um índice, o fator da forma do buraco (FFB)(18).
Observaram que o FFB é um fator prognóstico melhor que a medida da base interna isolada nas taxas de sucesso anatômico do BMI. Encontraram 80% de fechamento quando o FFB era maior que 0,9 e 25% quando o FBB era menor que 0,5. Entretanto, como a medida das bordas foram obtidas de forma oblíqua, a fidelidade dos resultados julgamos ficarem comprometidas.
Outros autores também utilizaram o FFB, observando que quando o FFB era maior que 0,9 o fechamento anatômico era de 100%, e quando era menor que 0,5 o fechamento era de apenas 67%(13).
Com relação ao coeficiente de correlação r, observaram que o diâmetro interno era melhor fator preditivo de fechamento que o FFB.
Foi demonstrado também, que nos BM estágios II e III de Gass, as medidas da altura e base externa do buraco poderiam ser usadas na criação de um índice (índice do buraco macular- IBM) com boa relação com a AV final(17).
Desde que a classificação do BMI foi proposta por Gass em 1988, sempre foi considerado na análise biomicroscópica, o tamanho da base interna do buraco. Baseado nos estudos acima citados e em nossa análise das medidas isoladas do OCT, julgamos que a base interna seria mais importante que a base externa na confecção de uma fórmula matemática, ou seja, um outro índice para tentar mimetizar o prognóstico anatômico e funcional de cada paciente antes da realização da cirurgia.
Na AV, o modelo estatístico apontou uma correlação positiva para a variável altura e uma correlação negativa para a variável base interna. A partir daí, criamos um índice dividindo a altura pela base interna do buraco.
O índice de prognóstico do buraco macular (IPBM) foi utilizado junto com outras variáveis como fator preditivo tanto de fechamento anatômico quanto de AV final.
Obteve-se por análise multivariada, que o índice IPBM é a variável mais importante dentre as variáveis significativas de fechamento anatômico (tempo, diâmetro da base interna e IPBM). Uma curva ROC identificou índices de corte para o IPBM entre <0,6 e >0,6, e através de regressão logística observamos que quando o IPBM é >0,6, o risco é 11 vezes maior de sucesso no fechamento anatômico do BMI.
A AV corrigida foi realizada ao final de seis meses de pós-operatório para evitar influência de cistos intraretinianos e fluído sub-retiniano que podem mascarar a AV antes deste período(22).
Todos os pacientes que desenvolveram catarata no decorrer do estudo, foram submetidos à facoemulsificação com implante de lente intra-ocular para não interferir nas medidas de acuidade visual.
Pacientes pseudofácicos que desenvolveram opacidade de cápsula posterior no decorrer do período foram submetidos à capsulotomia com Yag Laser.
Análise de regressão linear selecionou todas as variáveis significantes na AV final (BINT, IPBM e AV pré). Entre todas estas variáveis, o IPBM foi selecionado como o melhor preditor de AV final. O modelo aponta que entre estas variáveis significativas, o IBPM sozinho explica 41% da AV pós-operatória.
Em relação aos achados dos autores do IBM(17), algumas diferenças em relação ao nosso estudo são pertinentes: a maioria dos nossos BMI são do estágio IV, teoricamente os de pior prognóstico. A melhor resolução do OCT3 do que o OCT1, em se tratando de medidas tão tênues. A não utilização de ICG para realização da retirada da MLI, pois sua fototoxicidade ainda é discutida. A maioria dos BMI em nosso estudo (77,2%) têm IBM inferior a 0,5, segundo aquele autor, os de pior prognóstico.
As limitações em nossa análise incluem-se: o número ainda restrito de pacientes (n=22) já que estamos falando de um estudo piloto, 27,2% dos pacientes tinham pseudofacia prévia que altera o estado natural do vítreo, a grande maioria dos buracos maculares eram de estágio III e IV (95,5%), além do tempo de história ser maior que um ano em 59,1% dos casos.
Constatamos que entre as variáveis (idade, altura, diâmetro da base interna, diâmetro da base externa, tempo, AV pré, IBPM), o IBPM se apresentou como o melhor preditor de fechamento anatômico e acuidade visual pós-operatória.
CONCLUSÃO
Todo cirurgião deve atentar para as medidas da altura e da base interna dos buracos maculares na tomografia de coerência óptica. Acreditamos que quanto maior for a altura e menor for sua base interna, uma quantidade maior de tecido retiniano está disponível para o fechamento e talvez mais fotorreceptores estejam presentes para melhorar a acuidade visual final. Se a simples razão destas duas variáveis (IBPM) for superior a 0,6 tem-se um risco 11 vezes maior de sucesso no fechamento anatômico do BMI.
REFERÊNCIAS
1. Gass J. Idiopathic senile macular hole. Its early stages and pathogenesis. Arch Ophthalmol. 1988;106(5):629-39.
2. McDonnell PJ, Fine SL, Hillis AI. Clinical features of idiopathic macular cysts and holes. Am J Ophthalmol. 1982;93(6):777-86.
3. Gass J. Reappraisal of biomicroscopic classification of stages of development of a macular hole. Am J Ophthalmol. 1995;119(6):752-9.
4. Kelly NE, Wendel RT. Vitreous surgery for idiopathic macular holes. Results of a pilot study. Arch Ophthalmolol. 1991;109(5):654-9. Comment in: Arch Ophthalmol. 1991;109(5):635-6.
5. Huang D, Swanson EA, Lin CP, Schuman JS, Stinson WG, Chang W, et al. Optic coherence tomography. Science. 254(5035):1178-81.
6. Scott IU, Moraczewski AL, Smiddy WE, Flynn HW Jr, Feuer WJ. Long-term anatomic and visual acuity outcomes after initial anatomic success with macular hole surgery. Am J Ophthalmol. 2003;135(5):633-40.
7. Ezra E, Aylward WG, Gregor ZJ. Membranectomy and autologous serum for there treatment of full-thickness macular holes. Arch Ophthalmol. 1997;115 (10):1276-80.
8. Benson WE, Cruickshanks KC, Fong DS, Williams GA, Bloome MA, Framback DA, et al. Surgical management of macular holes: a report by the American Academy Ophthalmology. Ophthalmology. 2001;108(7):1328-35. Comment in: Ophthalmology. 2002;109(4):622-3.
9. Brooks HL Jr. Macular hole surgery with and without internal limiting membrane peeling. Ophthalmology. 2000;107(10):1939-48; discussion 1948-9.
10. Tranos PG, Ghazi-Nouri SM, Rubin GS, Adams ZC, Charteris DG. Visual function and subjective perception of visual ability after macular hole surgery. Am J Ophthalmol. 2004;138(6):995-1002.
11. Ip MS, Baker BJ, Duker JS, Reichel E, Baumal CR, Gangnon R, et al. Anatomical outcomes of surgery for idiopathic macular hole as determined by optical coherence tomography. Arch Ophthalmol. 2002;120(1):29-35.
12. Ulrich S, Haritoglou C, Gass C, Schaumberger M, Ulbiq MW, Kampik A. Macular hole size as a prognostic factor in macular hole surgery. Br J Ophthalmol. 2002;86(4):390-3.
13. Willis AW, Garcia-Cosio JF. Macular hole surgery: Comparison of longstanding versus recent macular holes. Ophthalmology. 1996;103(11):1811-4.
14. Smiddy WE, Thomley ML, Knighton RW, Feuer WJ. Use of the potential acuity meter and laser interferometer to predictive visual acuity after macular hole surgery. Retina. 1994;14(4):305-9.
15. Makino S, Inoda S, Shimizu Y, Shimizu H. [Results of vitreous surgery for idiopathic macular holes and retinal sensitivity]. Nippon Ganka Gakkai Zasshi. 1995;99(7):829-33. Japanese.
16. Terasaki H, Miyake Y, Tanikawa A, Kondo M, Ito Y, Horiguchi M. Focal macular electroretinograms before and after successful macular hole surgery. Am J Ophthalmol. 1998;125(2):204-13.
17. Kusuhara S, Teraoka Escano MF, Fujii S, Nakanishi Y, Tamura Y, Nagai A, et al. Prediction of postoperative visual outcome based on hole configuration by optical coherence tomography in eyes with idiopathic macular holes. Am J Ophthalmol. 2004;138(5):709-16. Comment in: Am J Ophthalmol. 2004; 138(5):845-6.
18. Desal VN, Hee MR, Puliafito CA. Optical coherence tomography of macular holes. In: Madreperla SA, McCuen BW, editors. Macular hole: pathogenesis, diagnosis and treatment. Oxford: Butterworth-Heinemann; 1999. p.37-47.
19. Costa RA, Calucci D, Skaf M, Cardillo JA, Castro JC, Melo LA Jr, et al. Optical coherence tomography 3: automatic delineation of the outer neural retinal boundary and influence on retinal thickness measurements. Invest Ophthalmol Vis Sci. 2004;45(7):2399-406.
20. Thompson JT, Smiddy WE, Glaser BM, Sjaarda RN, Flynn HW Jr. Intraocular tamponade duration and success of macular hole surgery. Retina. 1996;16(5): 373-82. Comment in: Retina. 1998;18(1):84-6; author reply 86-8.
21. Freeman WR, Azen SP, Kim JW, El-Haig W, Mishell DR 3rd, Bailey I. Vitrectomy for treatment of full-thickness stage 3 or 4 macular holes. Results of a multicentered randomized clinical trial. The Vitrectomy for Treatment of Macular Hole Study Group. Arch Ophthalmol. 1997;115(1):11-21. Erratum in: Arch Ophthalmol. 1997;115(5):636. Comment in: Arch Ophthalmol. 1997; 115(1):112; Arch Ophthalmol. 1997;115(9);1214-5.
22. Miura G, Mizunoya S, Arai M, Hayashi M, Yamamoto S. Early postoperative macular morphology and functional outcomes after successful macular hole surgery. Retina. 2007;27(2):165-8.
Endereço para correspondência:
Alan Diego Negretto
Rua Dona Avelina, 77/161
São Paulo (SP) CEP 04111-010
E-mail: [email protected]
Recebido para publicação em 25.05.2007
Última versão recebida em 14.06.2007
Aprovação em 18.06.2007
Nota Editorial: Depois de concluída a análise do artigo sob sigilo editorial e com a anuência do Dr. Eduardo Cunha de Souza sobre a divulgação de seu nome como revisor, agradecemos sua participação neste processo.
Trabalho realizado no Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo - USP.