Arq. Bras. Oftalmol. 2006; 69 (6): 10.1590/S0004-27492006000600004
Total: 2297
Núbia Cristina de Freitas Maia1; Wallace Chamon2; Bruno Castelo Branco3
DOI: 10.1590/S0004-27492006000600004
RESUMO
OBJETIVO: Avaliar a exeqüibilidade, eficácia e segurança do uso de microcerátomo e câmara anterior artificial para o transplante lamelar (sistema ALTK®). MÉTODOS: 21 olhos com opacidades corneanas superficiais foram submetidos ao transplante lamelar semi-automatizado de córnea. Nos olhos receptores a ceratectomia foi realizada de modo semelhante a uma cirurgia refrativa. As lamelas doadoras foram obtidas a partir de botões esclero-corneanos utilizando o mesmo microcerátomo e uma câmara anterior artificial. As medidas das espessuras corneanas foram feitas através da biomicroscopia ultra-sônica. RESULTADOS: As cirurgias obtiveram êxito em 19 olhos. Em 80% das lamelas obtidas em córneas doadoras e em 84,2% das lamelas em olhos receptores houve uma variação de até 0,5 mm do diâmetro desejado. Verificou-se alta semelhança entre as espessuras das lamelas obtidas nos olhos receptores e lamelas doadoras. Obteve-se acuidade visual corrigida pós-operatória igual ou superior a 20/40 em 52,6% dos olhos. Foram observadas complicações como diâmetro inadequado da lamela, perfuração intra-operatória no olho receptor e ectasia corneana pós-operatória (um caso). CONCLUSÕES: O transplante lamelar semi-automatizado de córnea mostrou-se exequível pela reprodutibilidade das espessuras e diâmetros das lamelas; eficaz pela melhora da acuidade visual pós-operatória e seguro, devido ao baixo índice de complicações cirúrgicas.
Descritores: Córnea; Câmara anterior; Opacidade da córnea; Ceratoplastia penetrante; Transplante de córnea; Doadores de tecido; Endotélio da córnea; Acuidade visual; Resultado de tratamento
ABSTRACT
PURPOSE: To evaluate the feasibility, efficacy and safety of a manual microkeratome and an artificial anterior chamber for lamellar keratoplasty (ALTK® system). METHODS: Twenty-one eyes with superficial corneal opacities were submitted to semi-automated lamellar keratectomy. In recipient eyes keratectomy was performed as in refractive surgery. The donor flap was removed from the preserved corneal shell using the same microkeratome and an artificial anterior chamber. Lamella thickness was measured through ultrasound biomicroscopy (UBM) after surgery. RESULTS: The surgeries were accomplished successfully in 19 eyes. 80% of the flaps obtained in donated corneas and 84.2% of the flaps in recipient eyes had an up to 0.5 mm variation variation of the desired diameter. A high similarity in flap thickness between the donor flap and the recipient cornea was obtained. Postoperative visual acuity of 20/40 or better was observed in 52.6% of the eyes. Complications such as undesired diameter of the flap, a case of perforation in the recipient eye and a case of cornea ectasia were observed. CONCLUSION: The semi-automated lamellar keratoplasty ALTK® system showed to be feasible due to the predictability and reproducibility regarding lamella thickness and diameter, efficient in the improvement of postoperative visual acuity and safe due to the low level surgical complication.
Keywords: Cornea; Anterior chamber; Corneal opacity; Keratoplasty; Corneal transplantation; Tissue donors; Endothelium corneal; Visual acuity; Treatment outcome
INTRODUÇÂO
A automatização da dissecção corneana não é uma idéia nova. O uso do microcerátomo para realização das ceratectomias em córneas doadoras e receptoras foi inicialmente citado por Barraquer, com o objetivo de conseguir um leito estromal uniforme(1). Outros autores também relataram resultados interessantes com o uso do microcerátomo de Barraquer, mas encontraram dificuldades em conseguir diâmetros semelhantes entre o botão doador e o leito receptor(2).
O desenvolvimento da cirurgia refrativa lamelar trouxe novas perspectivas para a ceratectomia: a possibilidade de utilizar os benefícios do corte regular do microcerátomo e a facilidade do seu manuseio na confecção de discos lamelares corneanos. Portanto, representou um grande avanço na técnica de obtenção de lamelas corneanas tanto em córneas doadoras quanto em córneas receptoras(1,3).
Com o aprimoramento das técnicas do LASIK e a melhoria da qualidade nos cortes dos microcerátomos, estes foram ganhando credibilidade quanto a sua eficiência e segurança(4-6).
Recentemente, uma nova câmara anterior artificial foi desenvolvida (ALTK System, Moria/Microtech). Esta câmara permite os cortes utilizando os botões corneoesclerais disponíveis nos bancos de olhos e o microcerátomo é acoplado facilmente(7-8).
Este estudo analisou o uso do microcerátomo e desta câmara anterior artificial nos transplantes lamelares de córnea como uma opção terapêutica para o tratamento de opacidades corneanas estromais superficiais, avaliando a exequibilidade, eficácia e segurança da ceratectomia.
MÉTODOS
Este estudo foi realizado no Departamento de Oftalmologia da Universidade Federal de São Paulo-Escola Paulista de Medicina (UNIFESP-EPM), devidamente aprovado pelo Comitê de Ética em Pesquisa da UNIFESP-EPM.
Os critérios de inclusão foram: opacidade corneana acometendo estroma anterior na área pupilar, espessura corneana central maior ou igual a 350 micra, acuidade visual igual ou melhor que percepção luminosa, ausência clínica de disfunção endotelial, indicação de transplante de córnea, inscrição na fila de espera do transplante de córnea. Pacientes que apresentavam alterações da superfície ocular associada à deficiência lacrimal, córneas com disfunção endotelial ou com grandes irregularidades de espessura foram excluídos do estudo.
Todos os pacientes foram submetidos a um exame oftalmológico completo incluindo acuidade visual potencial (PAM - Potential Acuity Meter Mentor®), biomicroscopia ultra-sônica e videoceratografia corneana.
As córneas doadoras foram disponibilizadas pelo Banco de Olhos do Hospital São Paulo. Foram utilizadas, preferencialmente, córneas sem viabilidade endotelial suficiente para transplante penetrante de córnea.
O sistema de ceratectomia lamelar automatizada utilizado (ALTK®, Automated Lamellar Therapeutic Keratectomy, Moria Inc., Antony, França) foi desenvolvido em 1997 e consiste em um microcerátomo de avanço manual, uma câmara anterior artificial para o preparo do botão doador e um sistema de apreensão do receptor (Figuras 1 e 2).


O microcerátomo consiste em uma cabeça de metal, de peça única conectado a uma turbina acoplada a tubulação de gás nitrogênio. Seu avanço é manual e existem diferentes cabeças, numeradas de acordo com a distância entre o corte da lâmina e a plataforma de aplanação. Conseqüentemente, quanto maior a distância entre a lâmina e a plataforma de aplanação, maior a numeração e maior a espessura do corte.
A câmara anterior artificial é um aparelho de metal, de desenho complexo, que permite a apreensão de botões córneo-esclerais (Figura 2). Consiste, didaticamente, em cinco partes(9): 1) Sistema de apreensão da córnea, que consiste em um pistão de perfil cônico, onde é apoiado a córnea, e um anteparo fixo que se encaixa em um anel inferior na base, apreendendo a córnea e vedando o sistema; 2) Sistema hidráulico de manutenção da pressão dentro da câmara anterior; 3) Sistema de apoio do anel guia do microcerátomo, que é composto por anel que serve de suporte para o anel guia do microcerátomo; 4) Anel guia do microcerátomo que apresenta um trilho para encaixe e deslizamento da cabeça do microcerátomo sobre a córnea. A altura do anel guia é regulada por meio do sistema de apoio e 5) Lentes de verificação do diâmetro por aplanação.
Os anéis de sucção para o receptor controlam a distância da córnea receptora à plataforma de aplanação do microcerátomo. Essa distância determina a quantidade de tecido corneano aplanado. Existem quatro anéis disponíveis com alturas diferentes (+2, +1, 0 e -1). O anel +2 é o mais alto e o anel -1 é o mais baixo, produzindo, para córneas de mesma curvatura, diâmetros menores e maiores, respectivamente. Como no doador, são utilizadas lentes de verificação do diâmetro do receptor por aplanação para confirmar a quantidade de tecido aplanado e estimar o diâmetro dos cortes a serem obtidos. Se necessário, o anel de sucção pode ser trocado até a obtenção do diâmetro aplanado desejado.
Após os exames pré-operatórios, o número da cabeça do microcerátomo foi escolhido embasado na espessura corneana total e na profundidade da opacidade do receptor. Todas as cirurgias foram realizadas sob anestesia loco-regional. O olho do receptor foi preparado primeiro, uma vez que os diâmetros dos botões doadores podiam ser controlados de maneira contínua pelo sistema de apoio do anel guia para ajustarem-se ao diâmetro obtido no receptor.
Preparação do receptor
O anel de sucção foi posicionado sobre o limbo e acionado o mecanismo de vácuo do aparelho para obtenção da apreensão do olho. A definição final do anel foi determinada por meio das lentes de verificação do diâmetro por aplanação e do diâmetro programado da ceratectomia. Após a confirmação da área aplanada, o anel foi irrigado com solução salina e o microcerátomo (já com a cabeça escolhida para a espessura programada do corte) foi encaixado no anel de sucção. Após o acionamento da oscilação da lâmina pelo pedal, o microcerátomo foi deslocado para frente pelo cirurgião, mantendo uma velocidade constante até que o tecido corneano fosse completamente retirado em forma de uma lamela. O corte total foi realizado em 3 a 4 segundos. Após a realização da ceratectomia, o diâmetro corneano retirado foi medido com um compasso cirúrgico para a calibração do diâmetro corneano do doador. Foi sempre considerado o maior diâmetro entre duas medidas em eixos ortogonais. A lamela, então, foi recolocada sobre o leito estromal e em seguida o botão doador foi preparado.
Preparação do doador
O botão córneo-escleral foi posicionado sobre a câmara anterior artificial e o sistema foi hermeticamente fechado. Para garantir uma boa pressão sob a córnea doadora, o frasco de solução salina conectado à câmara anterior artificial foi posicionado acima de 1 metro de altura, em relação à córnea. O epitélio do botão foi removido utilizando uma espátula e a pressão aferida com o tonômetro de Barraquer(10). Foi considerada uma boa pressão quando esta estava acima de 60 mmHg. As lentes aplanadoras foram, então, apoiadas sobre o suporte do anel guia do microcerátomo, para aferir o diâmetro da córnea aplanada. O suporte foi girado em sentido horário (para obter um diâmetro maior) ou no sentido anti-horário (para obter um diâmetro menor) até atingir o diâmetro programado (0,25 a 0,5 mm maior que o obtido no olho receptor). Uma vez regulado o suporte, o anel guia do microcerátomo foi posicionado e a ceratectomia foi então realizada com o mesmo número da cabeça do microcerátomo utilizado no receptor.
Após a colocação do tecido doador sobre o leito receptor, as suturas foram realizadas com fio de monofilamento de náilon 10-0. Ao final da cirurgia, em todos os casos, foram administradas injeções subconjuntivais de 1 ml de gentamicina 40 mg/ml e 1 ml de dexametasona 2 mg/ml. Os olhos foram ocluídos com curativos compressivos.
Pós-operatório
Foram administrados em todos os pacientes, colírios de antibiótico (Ofloxacino 0,3% - Alcon) e colírios de corticóide (Acetato de prednisolona 1% - Alcon) com posologia determinada, conforme a resposta inflamatória. As visitas pós-operatórias foram feitas após um dia, uma semana, um mês, dois meses, três meses, seis meses e um ano. Após o primeiro ano, as visitas passaram a ser anual. Os pontos frouxos foram retirados, quando necessário. Após o segundo mês de pós-operatório, os pacientes foram submetidos à retirada das suturas, embasado na videoceratografia.
Medidas das espessuras corneanas
Para medida pré-operatória da espessura da córnea e avaliação pré-operatória do leucoma ou da opacidade (profundidade) e para avaliação pós-operatória do transplante lamelar de córnea (determinação da espessura do botão transplantado e do leito receptor) foi utilizado a biomicroscopia ultra-sônica. O aparelho utilizado foi o Humphrey - UBM model 840 com transdutor de 50 MHz e excursão do transdutor de 5,5 mm.
Para medida da espessura total da córnea foi traçado um segmento de reta entre o eco referente à superfície anterior da córnea e o eco referente à superfície posterior da mesma. A interface entre o botão doador e o leito receptor foi facilmente detectada ao UBM como uma linha fina que separa uma porção estromal anterior mais homogênea e menos ecogênica (botão doador) de uma porção posterior geralmente mais ecogênica (leito receptor). A espessura do botão doador foi aferida traçando-se uma linha a partir do eco referente à interface até o eco referente à superfície anterior da córnea e a espessura do leito receptor (leito residual) foi medida a partir do eco da interface ao eco da face posterior da córnea.
A espessura da lamela retirada do olho receptor foi estimada subtraindo-se a medida do leito residual estromal pós-operatória da medida da espessura total corneana pré-operatória.
Metodologia estatística
Para análise da acuidade visual foi feita a conversão para LogMAR. As acuidades visuais aferidas pela tabela de Snellen foram convertidas para números decimais e calculado o negativo do logaritmo desses números, na base 10(11).
As análises foram realizadas utilizando-se os pacotes estatísticos Statistica 6.0 (StatSoft Inc., Tulsa, OK, EUA) e NCSS 2004 (Number Cruncher Statistical Systems, Kaysville, UT, EUA). Foi adotado 0,05 como nível de significância estatística.
RESULTADOS
Pacientes
Os dados pré-operatórios estão resumidos no quadro 1. Foram incluídos 21 olhos de 18 pacientes (6 mulheres e 12 homens), de maio de 1998 a julho de 2002. A idade variou de 18 a 70 anos (média de 51,8 anos, mediana 53 anos). A melhor acuidade visual corrigida por óculos pré-operatória foi de 20/70.
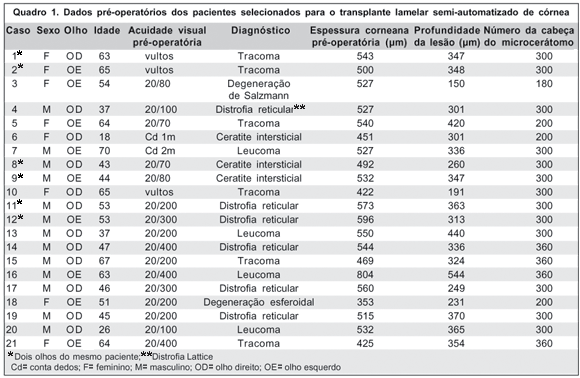
No pré-operatório, a profundidade da alteração estromal média foi de 324,8 µm (com variação de 150 a 544 µm, mediana de 336 µm), em córneas de espessura total média de 527,6 µm (com variação de 353 a 804 µm, mediana de 527 µm).
Diâmetro da lamela no receptor
O anel de sucção do receptor mais utilizado foi o anel +2 (80,9% dos pacientes). A escolha do anel de sucção final dependia da verificação do diâmetro aplanado.
Em dois pacientes, as ceratectomias não foram completadas. No caso 21, o corte foi incompleto devido à alta resistência ao avanço do microcerátomo, e, no caso 22, houve perfuração intra-operatória, sendo então cancelada a ceratectomia antes da sua finalização e suturada a própria córnea da paciente. Portanto, foram completadas 20 cirurgias em 19 olhos de 16 pacientes.
Quando comparada a medida aplanada pela lente de verificação do diâmetro e a medida do maior diâmetro obtido, 13 lamelas (68,4%) obtiveram o diâmetro exatamente como o aplanado. Em três pacientes, houve uma diferença de até 0,5 mm e em três pacientes esta diferença atingiu o valor máximo, ou seja, 1 mm (Figura 3). Um paciente não teve o diâmetro aplanado verificado previamente à ceratectomia e portanto não foi possível estabelecer a diferença entre os diâmetros (caso nº 4). Neste paciente o diâmetro obtido foi de 6 mm. Apesar do pequeno diâmetro, foi realizado o transplante. Após 3 meses, outro transplante foi realizado com diâmetro de 9 mm.
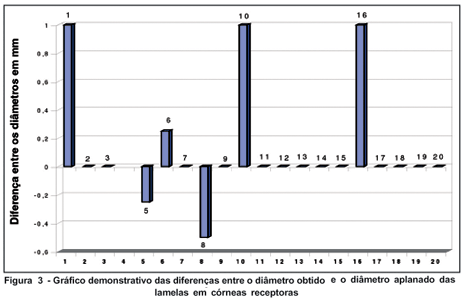
Diâmetro da lamela no doador
No total, foram realizadas 20 ceratectomias em córneas doadoras. Um paciente teve o mesmo olho reoperado com intervalo de 3 meses (caso 4). Neste caso foi utilizada na primeira cirurgia uma lamela de diâmetro pequeno (número 4) e na segunda cirurgia uma lamela de diâmetro maior, mais adequado para o transplante (número 20). Oito ceratectomias (40%) obtiveram exatamente o diâmetro aplanado e oito tiveram uma variação de até 0,5 mm e quatro (20%) tiveram uma diferença maior que 0,5 mm entre o diâmetro aplanado e o diâmetro obtido (Figura 4). Nos casos 6 e 10, houve a necessidade de trepanar a lamela doadora, adequando-a melhor ao diâmetro desejado. O botão doador, nos dois casos, teve um diâmetro maior que o desejado.
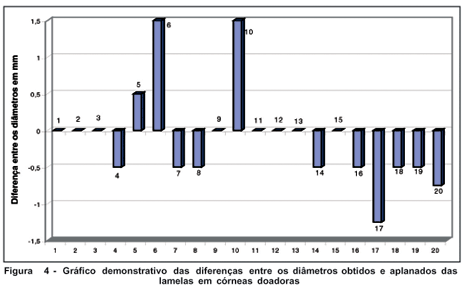
Na tentativa de avaliar a acurácia dos métodos de obtenção dos diâmetros em córneas receptoras e doadoras foi calculada uma variável denominada "desvio padrão do ideal" (calculado a partir da raiz quadrada de medida de variância). O valor do desvio padrão do ideal para o receptor foi de 0,45 mm e para o doador foi de 0,68 mm. Quanto menor o valor, melhor a acurácia. Entretanto, não foi encontrado diferença estatisticamente significante entre a acurácia na obtenção dos diâmetros das córneas receptoras e doadoras.
Medidas das espessuras corneanas
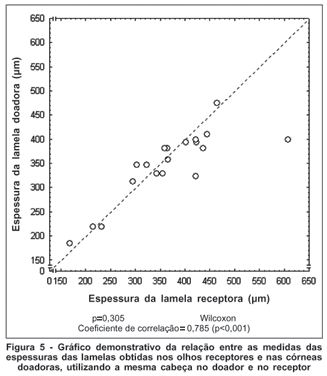
Na análise entre as espessuras das lamelas obtidas nos olhos receptores e córneas doadoras, não foi observada nenhuma diferença estatisticamente significante, mostrando uma alta correlação entre as espessuras dos cortes, independente da cabeça de microcerátomo utilizada (Figura 5). Das 20 ceratectomias realizadas com sucesso, 12 foram realizadas com a cabeça número 300. No olho receptor, a cabeça 300 cortou em média 377,2 micra e na córnea doadora 368,6 micra. Na maioria dos cortes com a cabeça 300, a espessura obtida foi superior a 300 micra (11 dos 12 cortes em olhos receptores e 100% das lamelas doadoras).
Acuidade visual
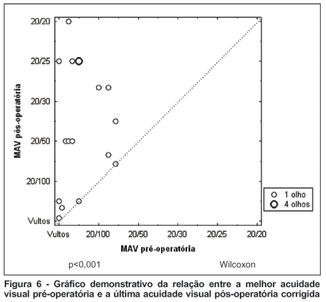
A maioria dos pacientes (89,5%) obteve uma acuidade visual pós-operatória melhor que a visão pré-operatória, sendo uma diferença estatisticamente significante (Figura 6). Dois olhos mantiveram a mesma visão pré e pós-operatória. Nenhum caso teve perda de linhas de visão.
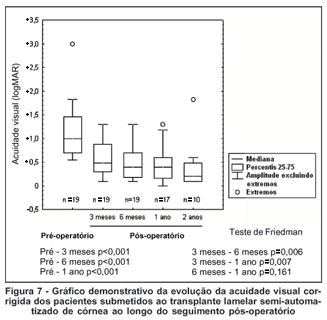
Ao longo do seguimento pós-operatório, houve diferença estatisticamente significante apenas entre a acuidade visual pré-operatória e a acuidade visual obtida aos 3 meses de pós-operatório. Nos meses seguintes, a acuidade visual praticamente manteve-se estável (Figura 7).
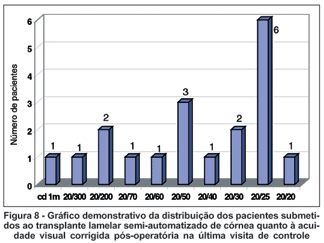
Dez olhos (52,6%) obtiveram uma acuidade visual pós-operatória melhor ou igual a 20/40. Nove olhos (47,4%) obtiveram uma acuidade visual na última visita inferior a 20/40 (Figura 8). Dentro desse grupo, em dois casos não foi possível aferir a visão potencial pré-operatória. No restante dos pacientes, um olho apresentava acuidade visual potencial de 20/400, dois olhos apresentavam 20/60, dois olhos apresentavam 20/50 e dois olhos tinham visão potencial de 20/30.
Complicações
Um olho (caso 4) foi operado duas vezes. Na primeira cirurgia, previamente à realização da ceratectomia no olho receptor, não foi aferido o diâmetro aplanado, e, conseqüentemente, houve um erro na escolha do anel de sucção e obteve-se uma ceratectomia de diâmetro muito pequeno. Apesar do diâmetro pequeno, o transplante foi realizado. Três meses após a primeira cirurgia, o paciente foi submetido novamente a cirurgia, respeitando todos os passos cirúrgicos, obtendo, então, uma ceratectomia de diâmetro adequado. A acuidade visual corrigida pós-operatória na última visita de controle era de 20/30.
Em um paciente (caso 21) não pôde ser completado a ceratectomia devido à dificuldade no avanço do microcerátomo. A resistência encontrada no movimento do microcerátomo impediu o avanço suave e completo, sendo então cancelado o procedimento e reposicionado a lamela com uma pequena sutura de contenção (4,8% dos casos). Não houve mudança na acuidade visual pós-operatória.
Uma paciente (caso 22) teve perfuração intra-operatória (4,8% dos casos), sendo então abortado o procedimento cirúrgico e suturada a própria córnea da paciente. A causa provável da perfuração intra-operatória foi a escolha errônea da cabeça do microcerátomo. Foi utilizada a cabeça número 360 para uma córnea com espessura total corneana de 425 micra. Alguns meses depois, a paciente foi submetida a um transplante penetrante de córnea.
Um caso evoluiu para ectasia corneana (caso 15). A partir do primeiro mês pós-operatório houve um aumento da ceratometria média. No exame clínico, constatou-se a presença de ectasia temporal, com área de afinamento do leito residual. No exame de biomicroscopia ultra-sônica foi observado leito residual do receptor de apenas 5 micra. A espessura total da córnea no pré-operatório era de 469 µm e a espessura do corte na córnea receptora foi de 464 µm. O número da cabeça do microcerátomo utilizado foi de 360 µm. Na última visita de controle, o paciente tinha uma acuidade visual pós-operatória corrigida com óculos de 20/200. Foi realizada uma adaptação de lente de contato rígida obtendo uma acuidade visual de 20/30.
Em alguns casos foram observados debris na interface, mas de pequena quantidade, fora da área pupilar. Em nenhum caso houve invasão de células epiteliais sob a lamela ou neovascularização da interface.
DISCUSSÃO
O presente estudo foi um dos pioneiros na utilização do sistema ALTK® na realização de transplantes lamelares de córnea, portanto, especial atenção foi dada na exequibilidade do procedimento.
Das 22 ceratectomias tentadas em receptores, 3 não foram bem sucedidas (2 casos de ceratectomia incompleta e uma perfuração intra-operatória - olhos nº 4, 21 e 22). Uma das mais importantes complicações no transplante lamelar é a perfuração intra-operatória. Neste estudo a perfuração intra-operatória ocorreu no olho receptor utilizando um microcerátomo de cabeça número 360 numa córnea de espessura total de 425 µm de uma paciente portadora de tracoma. Considerando o total de ceratectomias realizadas em olhos receptores, a incidência de perfuração intra-operatória neste estudo foi de 4,8% sendo uma das menores encontradas para o transplante lamelar de córnea. A incidência de perfuração encontrada na literatura oscila de zero a 30% e depende da técnica empregada(12-18). Das 20 ceratectomias realizadas em córneas doadoras, todas foram bem sucedidas, sendo que em 2 olhos o diâmetro obtido teve que ser corrigido por meio de trepanação manual (olho nº 6 e 10). Deve-se considerar que todos os botões corneanos utilizados para este estudo apresentavam um diâmetro total suficiente para que o sistema ficasse hermeticamente fechado. As córneas que não tinham diâmetro suficiente foram desprezadas.
O tempo cirúrgico da dissecção corneana, tanto nos pacientes receptores, quanto nas córneas doadoras, foi aproximadamente de 4 segundos cada. Ou seja, o uso do microcerátomo permitiu uma velocidade na cirurgia até então ainda não alcançada com nenhuma técnica de dissecção corneana. A facilidade do manuseio do microcerátomo permite que mesmo cirurgiões não muito experientes com cirurgia corneana tenham acesso a esta técnica.
Em 1988, alguns autores publicaram os resultados de transplantes lamelares de córnea utilizando o microcerátomo de Barraquer em globos oculares doadores inteiros. Os autores descreveram, principalmente, as dificuldades na confecção de discos lamelares de mesmo diâmetro, dificultando uma boa coaptação das bordas(19). Em 2001, outros autores descreveram bons resultados, sugerindo a utilização do microcerátomo como uma boa alternativa no tratamento das opacidades corneanas estromais anteriores(20).
O desenvolvimento de uma câmara anterior artificial permitiu aos cirurgiões o uso de discos córneo-esclerais preservados nos bancos de olhos, dispensando o uso de globos oculares inteiros. Há duas décadas, aproximadamente, uma câmara foi desenvolvida e permitiu o uso do microcerátomo de Barraquer para a ceratectomia em botões doadores preservados e fornecidos pelos bancos de olhos(21). No entanto, dois anos após, os próprios autores descreveram críticas sobre seu trabalho anterior devido principalmente à subestimação dos valores de espessura e do diâmetro do disco corneano(22).
Neste estudo, utilizando a câmara anterior artificial do sistema ALTK®, foi observado que 80% das lamelas obtidas das córneas doadoras tiveram uma variação de até 0,5 mm no diâmetro desejado. Quatro lamelas tiveram uma variação do diâmetro acima de 0,5 mm. Nos olhos receptores, 84,2% das lamelas obtidas tiveram uma variação de até 0,5 mm e a obtenção exata do mesmo diâmetro aplanado foi possível em 68,4% dos pacientes. Em três pacientes houve uma variação superior a 0,5 mm. A acurácia na obtenção dos diâmetros foi melhor nos olhos receptores, embora a diferença não tenha sido estatisticamente significante quando comparada com os diâmetros obtidos nas córneas doadoras.
A previsibilidade dos diâmetros é de fundamental importância, tanto para os resultados visuais quanto para uma melhor utilização das córneas doadoras. A boa coaptação das bordas, em decorrência de um diâmetro adequado dos botões corneanos e de uma ceratectomia regular, é um dos fatores que interfere na recuperação visual(1).
Em um estudo, onde foi avaliada a precisão dos cortes lamelares obtidos com o uso da câmara anterior artificial e microcerátomo, ambos fabricados pela Moria®, observou-se que 80% dos cortes em córneas doadoras tiveram o diâmetro com uma variação de até 0,5 mm do desejado(7). Isto demonstra alta acurácia, quando comparado com outras séries que mostravam uma variação maior que 1 mm(19,22). A análise morfológica feita por microscopia eletrônica de varredura revelou alta qualidade e regularidade da ceratectomia central e de suas margens. Nenhum outro método de dissecção (ar, fluido ou substância viscoelástica) foi capaz de obter a regularidade da superfície, reduzindo, então, os problemas da interface observados no transplante lamelar(7).
Numa outra análise da previsibilidade do diâmetro dos botões corneanos utilizando a câmara anterior artificial, os autores observaram que 90% dos cortes obtidos apresentavam um diâmetro com uma variação de até 0,25 mm do planejado(23).
Neste estudo, a espessura central média da lamela usando a cabeça de número 300, foi de 377,2±47,3 µm nos olhos receptores (mediana de 364,5 µm) e 368,6±31,9 µm nas córneas doadoras (mediana de 382 µm). A pressão da câmara anterior artificial, aferida com o tonômetro de Barraquer, momentos antes da ceratectomia da córnea doadora, era sempre acima de 60 mmHg.
Não foi encontrada na literatura específica referência quanto à espessura das lamelas obtidas nos olhos receptores utilizando o microcerátomo do sistema ALTK®. Relatos quanto à espessura das lamelas utilizando o microcerátomo nas cirurgias de LASIK mostram reprodutibilidade e segurança das ceratectomias. Numa análise das espessuras dos cortes em olhos receptores utilizando o microcerátomo Moria-LSK one com espessura programada de 160 micra foi encontrada uma média de 159 micra na região central das lamelas(24).
Numa análise de 47 ceratectomias em córneas doadoras, utilizando o sistema ALTK®, os autores observaram uma variação nas espessuras de cortes em córneas doadoras quando comparado o centro da lamela e sua periferia. Os botões corneanos obtidos eram mais espessos perifericamente que centralmente utilizando a cabeça número 180 e 300 micra. Os autores também observaram variações de espessuras regionais, ou seja, entre os quadrantes do botão. A espessura central dos botões com a cabeça número 300 com diâmetro de 9,0 mm foi de 217,4±72,2 µm. Os cortes foram realizados em uma câmara anterior artificial com pressão média de 53,5 mmHg(7).
Numa outra série de 25 ceratectomias lamelares com microcerátomo e utilizando a câmara anterior artificial com pressão de 65 mmHg, os autores observaram que 76% dos cortes em córneas doadoras apresentavam uma variação de até 100 micra na espessura estimada pelo número da cabeça do microcerátomo utilizada. Utilizando o microcerátomo com a cabeça 250 µm, os cortes tinham espessura central média de 256,7± 83,02 µm. Os autores também observaram que os cortes, utilizando a cabeça de número 350, eram mais espessos que o valor estimado(23).
Em um outro estudo realizado em 2002, avaliando a eficácia do microcerátomo e da câmara anterior artificial, os autores mostraram uma maior previsibilidade da espessura da lamela da córnea doadora quando o corte era realizado com uma pressão no interior da câmara anterior maior que a preconizada pelo fabricante (95,8±4,8 mmHg). Trabalhando com uma pressão maior, foi observada, também, uma melhor regularidade da espessura da lamela em toda sua extensão. A espessura central da lamela doadora com cabeça número 300 com o diâmetro de 8,0 mm foi de 280,7±34,6 µm e com o diâmetro de 9,0 mm foi e 296,5±31,3 µm(8).
Fatores como a variabilidade da hidratação corneana no post mortem, velocidade do avanço do microcerátomo, ângulo de ataque da lâmina, pressão inicial e a sua flutuação dentro da câmara anterior durante o movimento do microcerátomo deverão ser considerados e podem justificar a variação dos resultados(7-8,23,25-27).
Neste estudo, comparando as espessuras dos cortes nos olhos receptores e doadores, independente do número da cabeça de microcerátomo utilizada, foi observado alta similaridade entre as medidas. Não houve diferença estatisticamente significante entre as medidas de espessura (p=0,305). Observou-se também ausência de diferença estatisticamente significante entre as espessuras totais de córnea no pré-operatório e pós-operatório (p=0,3048).
Não foi encontrada na literatura nenhuma referência que evidencie a espessura dos cortes com o microcerátomo em olhos receptores e sua comparação com os olhos doadores.
A equivalência das espessuras dos cortes favorece os resultados visuais. O que é retirado do olho receptor deve ser reposto pela lamela doadora(1). Pequenas diferenças regionais de espessura dos botões, como encontrado em alguns estudos, podem interferir nos resultados visuais, caso essas mesmas diferenças não forem reproduzidas nos olhos receptores e doadores(7,23).
Há de se considerar que neste estudo, a ceratectomia nas córneas receptoras foi realizada em uma córnea sem edema, com epitélio muitas vezes íntegro. Já a ceratectomia nas córneas doadoras foi realizada em córneas com edema estromal e sem o epitélio. Considerando que o epitélio corneano tem uma espessura média de 50 micra(28-29), a sua retirada nas córneas doadoras é fundamental para manter uma espessura semelhante ao corte do receptor, pois há o processo de diminuição do edema da córnea doadora após alguns dias da cirurgia.
Quanto à acuidade visual, foi observado uma melhora estatisticamente significante da acuidade visual pós-operatória. A maioria dos pacientes (89,47%) apresentou melhora da acuidade visual pós-operatória. Apenas dois pacientes mantiveram a mesma acuidade visual que apresentavam no pré-operatório e nenhum paciente teve perda de linha de visão durante o seguimento pós-operatório. Dez pacientes (52,6%) obtiveram uma acuidade visual corrigida por óculos igual ou superior a 20/40 na última visita de controle.
Analisando a evolução da acuidade visual ao longo do pós-operatório, foi observado que houve uma melhora progressiva da acuidade visual até os 6 meses. A partir dos 6 meses de pós-operatório não foi observada diferença estatisticamente significante da acuidade visual. Com 12 meses de pós-operatório a média de acuidade visual corrigida encontrada foi de 20/43 (calculando a média em LogMar).
Varandas, numa análise de 32 olhos submetidos ao transplante lamelar semi-automatizado de córnea, relata uma melhora da acuidade visual corrigida em 75% dos casos, sendo os melhores resultados nos pacientes submetidos a uma dissecção mais profunda(30).
Numa série de 120 olhos submetidos a transplante lamelar profundo de córnea, a acuidade visual corrigida pós-operatória encontrada foi igual ou superior a 20/40 em 62,8% dos casos(15). Benson et al., constataram uma acuidade visual igual ou melhor que 20/30 em 73,8% dos 28 pacientes com ceratocone submetidos ao transplante lamelar(31).
Tsubota e colaboradores, observaram uma média de acuidade visual de 20/52 e justificaram o baixo resultado visual em decorrência das irregularidades da interface(16). Varandas, utilizando o microcerátomo, encontrou uma média de 20/35(30).
Vale ressaltar que um grande número de pacientes, neste estudo, apresentava baixa acuidade visual potencial (PAM). Deve ser considerado que, muitas vezes, a medida da visão potencial pode ter sido hipoestimada devido às irregularidades corneanas, já que não foi utilizada uma lente de contato rígida durante o exame(32-34); mas, alguns pacientes eram, provavelmente, portadores de ambliopia pois apresentavam história de opacidade corneanas desde a infância. Uma paciente, que teve os dois olhos operados, apresentava maculopatia miópica bilateral (olho nº 1 e 2). Outros pacientes deste estudo, devido à idade avançada, já apresentavam sinais de opacidade cristaliniana, fato este que também pode ter interferido nos resultados visuais.
Outros estudos mostram que a opacificação da interface, dobras no eixo visual, opacidade residual, ambliopia, além da catarata, são fatores que limitam o bom resultado visual nos transplantes lamelares.
Neste estudo, além das 3 ceratectomias nos olhos receptores que não foram concluídas corretamente (olhos nº 4, 21 e 22), um olho apresentou abaulamento progressivo corneano (olho nº 15).
Existem poucos relatos de ectasia corneana após transplante lamelar de córnea. As causas possíveis seriam a presença de ceratocone subclínico no botão doador ou um afinamento do botão devido a uma ação aumentada das colagenases(37). Neste estudo, um caso evoluiu com ectasia corneana após uma ceratectomia muito profunda no olho receptor, cuja medida da espessura do leito residual foi de apenas 5 micra. Apesar de ter sido reposto uma lamela doadora de espessura similar a que tinha se retirado do receptor, nos primeiros meses de pós-operatório observou-se um aumento da ceratometria média.
Todos os pacientes neste estudo tiveram melhora da transparência corneana e nenhum caso apresentou invasão epitelial na interface. Não se observou, até o último controle dos pacientes, nenhum caso de recidiva de distrofia corneana, opacificação da interface ou vascularização.
As pesquisas dos tratamentos cirúrgicos para restauração da função corneana, têm a cada dia, avançado e se aperfeiçoado através do uso de microcerátomos e também do excimer laser. Futuramente, técnicas sofisticadas, de manuseio fácil e de baixo custo estarão disponíveis e acessíveis a todos, visando um melhor aproveitamento das córneas doadas e diminuindo a lista de espera dos pacientes.
CONCLUSÕES
O transplante lamelar semi-automatizado de córnea foi realizado com sucesso em 86,3% dos olhos.
A exequibilidade do tratamento foi comprovada pela reprodutibilidade das espessuras corneanas e dos diâmetros das lamelas corneanas tanto em córneas doadoras quanto receptoras.
A eficácia do tratamento foi comprovada com a melhora da acuidade visual em 89,5% dos casos, obtendo-se uma acuidade visual pós-operatória igual ou superior a 20/40 em 52,6% (10/19) dos olhos operados.
A segurança observada neste estudo foi demonstrada pela ausência da diminuição da acuidade visual com correção e pela baixa incidência de complicações, não piorando o prognóstico para um segundo transplante, lamelar ou penetrante.
REFERÊNCIAS
1. Barraquer JI. Lamellar keratoplasty. (Special techniques). Ann Ophthalmol. 1972;4(6):437-69.
2. Hanna KD, David T, Besson J, Pouliquen Y. Lamellar keratoplasty with the Barraquer microkeratome. Refract Corneal Surg. 1991;7(2):177-81.
3. Wong DW, Chan WK, Tan DT. Harvesting a lamellar graft from a corneoscleral button: a new technique. Am J Ophthalmol. 1997;123(5):688-9.
4. Pallikaris IG, Papatzanaki ME, Stathi EZ, Frenschock O, Georgiadis A. Laser in situ keratomileusis. Lasers Surg Med. 1990;10(5):463-8.
5. Pallikaris IG, Papatzanaki ME, Siganos DS, Tsilimbaris MK. A corneal flap technique for laser in situ keratomileusis. Human studies. Arch Ophthalmol. 1991;109(12):1699-702.
6. Buratto L, Ferrari M, Rama P. Rama, Excimer laser intrastromal keratomileusis. Am J Ophthalmol. 1992;113(3):291-5.
7. Behrens A, Dolorico AM, Kara DT, Novick LH, McDonnell PJ, Chao LC, et al. Precision and accuracy of an artificial anterior chamber system in obtaining corneal lenticules for lamellar keratoplasty. J Cataract Refract Surg. 2001;27 (10):1679-87.
8. Li L, Behrens A, Sweet PM, Osann KE, Chuck RS. Corneal lenticule harvest using a microkeratome and an artificial anterior chamber system at high intrachamber pressure. J Cataract Refract Surg. 2002;28(5):860-5. Comment in: J Cataract Refract Surg. 2003;29(1):5-6; author reply 6.
9. Chamon, W. Restauração da função corneana: ceratectomia fototerapêutica e transplante lamelar automatizado de córnea como alternativas ao transplante penetrante de córnea (tese). São Paulo: Universidade Federal de São Paulo; 2000.
10. Barraquer JI. New applanation tonometer for operating room. Ophthalmologica. 1967;153(3):225-8.
11. Holladay JT. Proper method for calculating average visual acuity. J Refract Surg. 1997;13(4):388-91.
12. Amayem AF, Anwar M. Fluid lamellar keratoplasty in keratoconus. Ophthalmology. 2000;107(1):76-9; discussion 80. Comment in: Ophthalmology. 2001;108(6):1010-1.
13. Francesconi CM. Forseto AS, Nosé RM, Nosé W. Ceratoplastia lamelar profunda com viscodissecção da membrana de Descemet. Arq Bras Oftalmol. 2001; 64(5):385-8.
14. Melles GR, Remeijer L, Geerards AJ, Beekhuis WH. A quick surgical technique for deep, anterior lamellar keratoplasty using visco-dissection. Cornea. 2000;19(4):427-32.
15. Sugita J, Kondo J. Deep lamellar keratoplasty with complete removal of pathological stroma for vision improvement. Br J Ophthalmol. 1997;81(3):184-8. Comment in: Br J Ophthalmol. 1997;81(3):178-9. Br J Ophthalmol. 1998;82 (2):205.
16. Tsubota K, Kaido M, Monden Y, Satake Y, Bissen-Miyajima H, Shimazaki J. A new surgical technique for deep lamellar keratoplasty with single running suture adjustment. Am J Ophthalmol. 1998;126(1):1-8.
17. Price FW Jr. Air lamellar keratoplasty. Refract Corneal Surg. 1989;5(4):240-3.
18. Anwar M, Teichmann KD. Big-bubble technique to bare Descemet's membrane in anterior lamellar keratoplasty. J Cataract Refract Surg. 2002;28(3):398-403. Comment in: J Cataract Refract Surg. 2002;28(12):2067; author reply 2067-8.
19. Hanna K, Saragoussi JJ, David T, Pouliquen Y. [Lamellar keratoplasty with the Barraquer microkeratome. Preliminary clinical study apropos of 7 cases] J Fr Ophtalmol. 1988;11(5):419-23. French.
20. Jimenez-Alfaro I, Perez-Santonja JJ, Gomez Telleria G, Bueno Palacin JL, Puy P. Therapeutic lamellar keratoplasty with an automated microkeratome. J Cataract Refract Surg. 2001;27(8):1161-5.
21. Maguen E, Villasenor RA, Ward DE, Nesburn AB. A modified artificial anterior chamber for use in refractive keratoplasty. Am J Ophthalmol. 1980;89(5): 742-4.
22. Maguen E, Azen SP, Pinhas S, Villasenor RA, Nesburn AB. Evaluation of sources of variation on the accuracy and reproducibility of microkeratome sections with the modified artificial anterior chamber. Ophthalmic Surg. 1982;13 (3):217-20.
23. Springs CL, Joseph MA, Odom JV, Wiley LA. Predictability of donor lamellar graft diameter and thickness in an artificial anterior chamber system. Cornea. 2002;21(7):696-9.
24. Jacobs BJ, Deutsch TA, Rubenstein JB. Reproducibility of corneal flap thickness in LASIK. Ophthalmic Surg Lasers. 1999;30(5):350-3.
25. Kim YH, Choi JS, Chun HJ, Joo CK. Effect of resection velocity and suction ring on corneal flap formation in laser in situ keratomileusis. J Cataract Refract Surg. 1999;25(11):1448-55.
26. Seo KY, Wan XH, Jang JW, Lee JB, Kim MJ, Kim EK. Effect of microkeratome suction duration on corneal flap thickness and incision angle. J Refract Surg. 2002;18(6):715-9.
27. Wachtlin J, Schrunder S, Pham DT, Hoffmann F, Hartmann C. [Rise in intraocular tension in microkeratome sections (LASIK) and with the GTS trephine system for keratoplasty]. Ophthalmologe. 1998;95(3):137-41. German.
28. Reinstein DZ, Silverman RH, Rondeau MJ, Coleman DJ. Epithelial and corneal thickness measurements by high-frequency ultrasound digital signal processing. Ophthalmology. 1994;101(1):140-6.
29. Li HF, Petroll WM, Moller-Pedersen T, Maurer JK, Cavanagh HD, Jester JV. Epithelial and corneal thickness measurements by in vivo confocal microscopy through focusing (CMTF). Curr Eye Res. 1997;16(3):214-21.
30. Varandas VS. Estudo da eficácia da ceratoplastia lamelar automatizada (tese). Rio de Janeiro: Universidade Federal do Rio de Janeiro; 2003.
31. Benson WH, Goosey CB, Prager TC, Goosey JD. Visual improvement as a function of time after lamellar keratoplasty for keratoconus. Am J Ophthalmol. 1993;116(2):207-11.
32. Smiddy WE, Horowitz TH, Stark WJ, Klein P, Kracher GP, Maumenee AE. Potential acuity meter for predicting postoperative visual acuity in penetrating keratoplasty. A new method using a hard contact lens. Ophthalmology. 1987; 94(1):12-6.
33. Barkana Y, Segal O, Krakovski D, Avni I, Zadok D. Prediction of visual outcome after penetrating keratoplasty for pseudophakic corneal edema. Ophthalmology. 2003;110(2):286-90.
34. Bosse JC. Potential visual acuity measured with and without pupil dilation. Optom Vis Sci. 1989;66(8):537-9.
35. Soong HK, Katz DG, Farjo AA, Sugar A, Meyer RF. Central lamellar keratoplasty for optical indications. Cornea. 1999;18(3):249-56.
36. Saini JS, Jain AK, Sukhija J, Saroha V. Indications and outcome of optical partial thickness lamellar keratoplasty. Cornea. 2003;22(2):111-3.
37. Patel N, Mearza A, Rostron CK, Chow J. Corneal ectasia following deep lamellar keratoplasty. Br J Ophthalmol. 2003;87(6):799-800.
Endereço para correspondência:
Nubia Cristina de Freitas Maia
507 sul - Alameda 8 - Lote 3 - Casa 3
Palmas (TO) CEP 77000-000
E-mail: [email protected]
Recebido para publicação em 03.10.2005
Última versão recebida em 28.05.2006
Aprovação em 01.06.2006
Trabalho realizado na Universidade Federal de São Paulo - UNIFESP.
Nota Editorial: Depois de concluída a análise do artigo sob sigilo editorial e com a anuência dos Drs. Breno Barth Amaral de Andrade e José Américo Bonatti sobre a divulgação de seus nomes como revisores, agradecemos sua participação neste processo.
How to cite this article: