
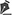
Sílvia Ligório Fialho1; Marcelo Guimarães Brandão Rego2; José Augusto Cardillo2; Rubens Camargo Siqueira; Rodrigo Jorge3; Armando da Silva Cunha Júnior1
DOI: 10.1590/S0004-27492003000700029
RESUMO
O tratamento de doenças oculares que acometem o vítreo e a retina tem sido um problema devido à dificuldade de penetração das drogas no segmento posterior do bulbo ocular. A administração de colírios apresenta efeito terapêutico mínimo nessa região do olho, que, geralmente, é mantido com a administração de doses freqüentes do medicamento. Uma alternativa seria a injeção intra-ocular; entretanto, a rápida circulação sangüínea nesses locais promove uma redução da meia-vida das drogas, diminuindo, rapidamente, suas concentrações a níveis subterapêuticos. Visando a obtenção de níveis terapêuticos adequados de drogas no segmento posterior do bulbo ocular por longos períodos, sistemas de liberação poliméricos implantados intravítreo estão sendo investigados para o tratamento de várias doenças vítreo-retinianas. Esses implantes são preparados a partir de diferentes polímeros, os quais podem ser biodegradáveis ou não biodegradáveis. Os polímeros derivados dos ácidos lático e glicólico têm se revelados bastante promissores devido, principalmente, às suas características de biocompatibilidade e biodegradabilidade. De acordo com os estudos realizados até o momento, os implantes podem se apresentar na forma de bastão, de discos ou de membranas e ser obtidos pelos métodos de moldagem, de extrusão ou de preparação de filmes. O presente artigo objetiva uma revisão de literatura abordando o tema e os principais estudos relacionados com a utilização de implantes poliméricos como sistemas transportadores de drogas para aplicação intra-ocular.
Descritores: Implantes de medicamento; Implantes absorvíveis; Sistemas de liberação de medicamentos; Preparações de ação retardada; Tecnologia farmacêutica
ABSTRACT
The treatment of vitreoretinal disorders has been problematic because it is difficult to gain access to the posterior segment of the eye. Topical instillation of eye drops has little therapeutic effect on posterior structures which cannot be maintained without frequent administration. Intraocular injections could be an alternative, but the fast flowing blood supply in this region, associated with the rapid clearance rates, causes the drug concentration to fall rapidly below therapeutic levels. In order to obtain therapeutic levels over longer time periods, polymeric sustained-drug release systems, implanted into the vitreous, are being studied for the treatment of vitreoretinal disorders. These systems are prepared using different kinds of polymers that can be biodegradable or nonbiodegradable. The polymers derived from lactic and glycolic acids have been the most promising for drug delivery systems because of their biocompatibility and biodegradation. According to previous studies, the polymers can be manufactured in the form of rods, discs or membranes, using the following methods: molding, extrusion or preparation of films. In this review, we present the technology and some preliminary studies of biodegradable implants in relation to intraocular drug delivery systems.
Keywords: Drug implants; Absorbable implants; Drug delivery system; Delayed-action preparations; Technology, pharmaceutical
INTRODUÇÃO
O tratamento de doenças oculares que acometem o vítreo e a retina, estruturas do segmento posterior do bulbo ocular, tem sido um problema devido à dificuldade de penetração nesse segmento do olho. A administração de colírios, embora seja o método mais empregado, apresenta efeito terapêutico mínimo na região posterior do olho, que, geralmente, é mantido com aplicações freqüentes da formulação. A via sistêmica pode ser utilizada com essa finalidade, mas, também se observa baixa penetração no olho em virtude da existência da barreira hematorretiniana, que dificulta a entrada de substâncias da circulação sangüínea para a retina. Portanto, para que se obtenha uma concentração da droga dentro da faixa terapêutica utilizando essa via, é necessária a administração de concentrações elevadas durante um período prolongado, podendo ocasionar sérios efeitos adversos em outros órgãos do corpo humano. A injeção intra-ocular seria uma alternativa para a obtenção da concentração adequada no vítreo e na retina. Mas a rápida circulação sangüínea nesses locais promove uma redução da meia-vida das drogas nos mesmos, reduzindo, rapidamente, suas concentrações a níveis subterapêuticos. Para que os níveis se mantenham dentro da faixa terapêutica, são necessárias, então, injeções repetidas no interior da cavidade vítrea, as quais podem causar desconforto para o paciente e ocasionar complicações como hemorragia vítrea, infecções, catarata e descolamento da retina(1-2).
Por causa das razões acima descritas, têm sido realizados diversos estudos visando o desenvolvimento de sistemas que sejam capazes de manter a concentração das drogas no segmento posterior do olho, dentro do nível terapêutico, por um período mais prolongado(3). Os antiinflamatórios esteróides têm merecido atenção especial, pois desempenham papel importante no tratamento de diversas doenças oculares que envolvam inflamação e proliferação fibrovascular.
Sistemas de liberação controlada, como as microesferas e os lipossomas, estão em estudo com o objetivo de melhorar o tratamento por meio da manutenção da concentração e do aumento da liberação da droga no local de aplicação e da redução da toxicidade intra-ocular. Entretanto, existem alguns obstáculos relacionados à complexidade dos métodos de preparação e à dificuldade de esterilização, que limitam a utilização desses sistemas. Além disso, ao serem administradas, as partículas presentes nessas formulações se encontram suspensas na cavidade vítrea, causando embaçamento da visão do paciente e dificultando o exame de fundo de olho pelo oftalmologista(4). Por causa de problemas decorrentes do uso das microesferas e dos lipossomas, estão em desenvolvimento, recentemente, implantes capazes de promover a liberação prolongada de drogas no interior do olho.
Estrutura e tipos de polímeros utilizados no preparo de implantes
Como o sistema de liberação de droga na forma de implante deve ser biocompatível com o organismo, os componentes nele presentes devem ser quimicamente inertes, não-carcinogênicos, hipoalergênicos, mecanicamente estáveis e não-causadores de resposta inflamatória no local de aplicação. Acrescenta-se, ainda, que as características químicas e físicas do material não devem ser modificadas pelo tecido local(5).
Os implantes são preparados a partir de diferentes polímeros, os quais podem ser biodegradáveis ou não-biodegradáveis, podendo ser de dois tipos: matriciais (ou monolíticos) e reservatórios(1,6).
No sistema matricial, a droga se encontra homogeneamente dispersa na matriz polimérica ou adsorvida na superfície, e a sua liberação ocorre por difusão pelos poros da matriz, por degradação do polímero ou por uma combinação dos dois mecanismos. Caso a velocidade de degradação do polímero seja inferior à difusão da droga pela matriz, a liberação inicial dessa é dependente de sua difusão pelo sistema, podendo diferir se ela estiver dissolvida molecularmente ou dispersa no polímero. Quando se utilizam polímeros não-biodegradáveis, a liberação ocorre apenas por um processo de difusão lenta pela matriz.
No sistema do tipo reservatório, a droga se encontra em uma cavidade central envolta por uma membrana polimérica, a qual controla sua taxa de liberação. Mudanças na natureza e espessura dessa membrana promovem alterações na velocidade de liberação das drogas. Da mesma maneira que no sistema matricial, no sistema reservatório composto por polímeros não-biodegradáveis a liberação da droga ocorre apenas por difusão através da membrana.
Sistemas compostos por polímeros não-biodegradáveis, principalmente, os derivados de celulose, silicones, polímeros acrílicos, polivinilpirrolidona e copolímeros dos óxidos de etileno e propileno, embora apresentem uma taxa de liberação relativamente constante, precisam ser removidos posteriormente, o que requer processos cirúrgicos. Já os biodegradáveis podem apresentar vantagens sobre os anteriores, pois são totalmente absorvidos pelo organismo, não necessitando remoção subseqüente e proporcionando melhor adesão e aceitação do paciente ao tratamento(1). A preparação de sistemas biodegradáveis, no entanto, requer o controle de um maior número de variáveis já que a cinética de degradação do polímero in vivo deve permanecer constante para que seja obtida uma liberação controlada da droga. Portanto, é necessário que fatores como o pH e a temperatura, que podem promover um aumento ou uma redução na velocidade de degradação do implante, precisem ser avaliados durante o desenvolvimento(6).
Polímeros biodegradáveis naturais e sintéticos estão sendo estudados como componentes em sistemas de liberação de drogas, mas apenas alguns têm demonstrado verdadeira biocompatibilidade(7). Os naturais, à base de proteínas, como as albuminas bovina e humana, o colágeno e a gelatina, apresentam uso restrito por conterem pureza questionável e, em alguns casos, atividade antigênica marcante. Já os sintéticos, representados por poliamidas, poliaminoácidos, polialquilcianacrilatos, poliésteres, poliortoésteres, poliuretanos e poliacrilamidas, têm apresentado crescente interesse na aplicação como sistemas de liberação de drogas. Os polímeros biodegradáveis mais utilizados atualmente são os poliésteres, tais como a poli(e-caprolactona), o poli(D,L-lático) (PLA) e os copolímeros derivados dos ácidos lático e glicólico (PLGA), sendo que os dois últimos tipos têm sido amplamente empregados.
Polímeros e copolímeros derivados dos ácidos lático e glicólico
Durante o final da década de 60 e início da década de 70, foram realizados diversos estudos relacionados com a utilização dos polímeros derivados dos ácidos lático e glicólico para a fabricação de fios de sutura. Os resultados mostraram que eles proporcionaram boas propriedades mecânicas, baixa capacidade alergênica, baixa toxicidade, excelente biocompatibilidade e uma cinética previsível de biodegradação, despertando a atenção de vários pesquisadores quanto a suas possíveis aplicações em tecnologia farmacêutica. Essas substâncias obtiveram aprovação pelo Food and Drug Administration (FDA) para a utilização como sistemas de liberação de drogas, existindo diversos estudos demonstrando sua baixa toxicidade(7).
Os polímeros e copolímeros derivados dos ácidos lático e glicólico são sintetizados por uma reação de condensação, através da abertura do anel dos dímeros cíclicos (ácido lático e/ou ácido glicólico). A polimerização geralmente ocorre por um período de duas a seis horas, sob temperatura em torno de 175º C, utilizando, como catalisador, principalmente, o cloreto estanhoso. Durante o processo, pode ser adicionado álcool laurílico para controlar a massa molecular.
O ácido lático possui um carbono beta assimétrico que permite a obtenção das formas levógiras (L-PLA), dextrógiras (D-PLA) ou racêmicas (D,L-PLA), sendo que as formas levógiras e dextrógiras são semicristalinas, graças à elevada regularidade da cadeia polimérica, e as formas racêmicas são amorfas por apresentarem irregularidades na estrutura da cadeia do polímero(8). Logo, prefere-se a utilização de D,L-PLA já que esta forma permite uma dispersão mais homogênea da droga na matriz polimérica.
A biodegradação desses polímeros ocorre por erosão, por meio de clivagem da cadeia polimérica por hidrólise, liberando os ácidos lático e glicólico (Figura 1). Esses ácidos, por serem metabólitos naturais do organismo, são eliminados pelo ciclo de Krebs na forma de gás carbônico e água(5). O papel de atuação das enzimas na biodegradação do PLGA e PLA ainda não se encontra bem definido, embora dados descritos na literatura afirmem que esse processo não implica qualquer atividade enzimática, sendo a hidrólise o único mecanismo envolvido(9).
A presença do grupo metila (CH3) no polímero derivado do ácido lático confere a este uma maior hidrofobicidade quando comparado ao derivado do ácido glicólico (PGA). O PGA, portanto, por ser bastante sensível à hidrólise, não é adequado para a utilização em sistemas de liberação de drogas. Com relação ao PLGA, quanto maior a proporção de ácido lático, maior a hidrofobicidade do copolímero, já que absorve menos água, e conseqüentemente, menor será a velocidade de degradação. Além disso, a massa molecular e o grau de cristalinidade podem influenciar as propriedades mecânicas, a capacidade de hidrólise e a velocidade de degradação desses polímeros(10-11). Os principais fatores responsáveis por alterações no período de degradação dos polímeros biodegradáveis são: estrutura química e composição do sistema; distribuição da massa molecular dos polímeros; presença de monômeros e oligômeros; tamanho e forma da superfície do sistema; morfologia dos componentes do sistema (amorfo, semicristalino, cristalino); local de implantação do sistema e mecanismo de hidrólise.
A temperatura de transição vítrea (Tg) dos diferentes PLA e PLGA se encontra acima da fisiológica (37°C) e, nessa condição, eles se encontram na forma cristalina. Desse modo, a cadeia se apresenta como uma estrutura relativamente rígida, proporcionando uma força mecânica significativa e permitindo que sejam formulados como sistemas de liberação de drogas(7). Essa característica é, também, um fator determinante da velocidade de degradação dos polímeros já que está relacionada ao grau de cristalinidade e à organização das cadeias poliméricas. Portanto, o polímero que apresenta maior Tg, geralmente se degrada mais lentamente. O PGA apresenta temperatura de transição vítrea inferior (ou até mesmo próxima) à corporal, sendo este um outro fator que o torna inadequado com relação à sua utilização em sistemas de liberação de drogas. As propriedades desses polímeros podem ser observadas na tabela 1.
Os polímeros descritos podem ser utilizados na preparação de implantes, os quais se apresentam, geralmente, na forma de bastão, discos ou membranas. Os métodos de obtenção desses sistemas incluem: a moldagem, a extrusão e a preparação de filmes. Através da moldagem, a mistura de pós (contendo o polímero e a droga) previamente liofilizada é colocada em um molde desenvolvido na forma do implante, e podem ser utilizados o aquecimento e a pressão. Na extrusão, a mistura de pós é propulsionada continuamente pelo equipamento, passando por regiões de alta temperatura e pressão, onde ela é fundida e compactada na forma final do implante. A preparação de filmes pode ser realizada através de fusão e pressão da mistura de pós ou por adição da solução. O método de adição da solução é o mais utilizado, e, nele, os componentes são dissolvidos em um solvente apropriado formando uma solução que é, então, lançada sobre uma superfície lisa e não-adesiva. O solvente se evapora, e o filme formado é retirado da superfície(1).
A esterilização de implantes contendo polímeros derivados dos ácidos lático e glicólico tem sido um grande objeto de estudo. A esterilização terminal e a preparação em ambientes assépticos são os métodos mais descritos na literatura(5,7). Para que não sejam provocadas alterações nas propriedades físicas e mecânicas dos polímeros e, conseqüentemente, no seu perfil in vivo é muito importante a escolha da técnica adequada.
A esterilização por autoclave é um método que não pode ser utilizado para os polímeros acima descritos, já que condições de alta pressão e temperatura promovem deformação e hidrólise da matriz polimérica devido à natureza termoplástica do PLGA e PLA. As temperaturas utilizadas, por serem superiores à temperatura de transição vítrea dos polímeros, promovem alterações físicas e mecânicas dos sistemas.
A radiação através de raios gama (raios g) tem sido bastante estudada. Ao se submeterem os polímeros a esse tipo de método, ocorre uma quebra da cadeia polimérica, redução da viscosidade intrínseca, aumento da velocidade de erosão in vitro e in vivo, além do aumento da cinética de liberação da droga. Esses fatores, que limitam a utilização desse método, são dependentes da dose de radiação aplicada.
A esterilização química, empregando gases como o óxido de etileno, pode ser utilizada nos casos em que os polímeros são sensíveis à temperatura e umidade. Entretanto, resíduos de gás podem ser encontrados na superfície ou no interior da matriz polimérica, os quais são mutagênicos, carcinogênicos e alergênicos. Nesse processo, é essencial que o sistema seja submetido à degaseificação ou à aeração subseqüente para que os níveis de óxido de etileno se reduzam a valores aceitáveis, o que torna o método bastante lento.
Desse modo, a preparação dos implantes em ambiente asséptico torna-se o método mais seguro e eficaz. Os polímeros são facilmente solúveis em diferentes solventes orgânicos, de modo que a solução resultante pode ser submetida a uma filtração esterilizante sob fluxo laminar.
Aplicações e estudos
Os sistemas poliméricos podem ser implantados em diferentes regiões do olho humano. Ordenando-se as regiões da mais superficial a mais profunda, temos: região subconjuntival, região subtenoniana, esclera e o interior do globo ocular (câmara anterior e cavidade vítrea)(1). Em geral quanto mais profunda a região, mais delicado o procedimento e mais eficaz a concentração no vítreo e na retina.
Com a finalidade de se obterem níveis terapêuticos adequados da droga no segmento posterior do bulbo ocular, sistemas de liberação de drogas implantados intravítreo e preparados a partir de polímeros biodegradáveis (principalmente os derivados dos ácidos lático e glicólico) estão sendo investigados em várias doenças dentre as quais pode-se destacar: proliferação vítreo-retiniana (PVR)(12-14), retinite causada por citomegalovírus (CMVR)(15), endoftalmites(16), uveítes(17), degeneração macular relacionada à idade(18-19), retinopatia diabética(20) e edema macular pós-operatório(21). A liberação de drogas de forma contínua durante semanas ou meses pode ser determinante no prognóstico de várias doenças vítreo-retinianas, pois mantém níveis terapêuticos enquanto persiste o estímulo causador dessas, ou até a sua cura. Entretanto, ainda são necessários maiores estudos in vivo com relação ao perfil de liberação e a segurança desses sistemas. A fluocinolona em sistemas não biodegradáveis e a dexametasona em sistemas biodegradáveis já estão em fase III de estudos clínicos nos Estados Unidos. Recentemente o potencial da triamcinolona também tem sido avaliado em estudos clínicos(20,22).
Kimura e colaboradores desenvolveram dois implantes biodegradáveis à base de D,L-PLA, sendo que um deles era composto pelo polímero de peso molecular de 5600 Daltons (implante 1) e o outro pelo de 9100 Daltons (implante 2)(23). Ambos continham fluoresceína sódica (NaF), na concentração de 10%, como marcador hidrofílico. Nesse trabalho, foi avaliado o perfil de liberação in vitro e a cinética in vivo do marcador, após implantação intravítrea. Os implantes 1 e 2 liberaram NaF, in vitro, por mais de 25 e 45 dias, respectivamente. Concentrações detectáveis do marcador foram encontradas no vítreo de coelhos após 17 dias (implante 1) e 28 dias (implante 2). Os dois sistemas apresentaram boa tolerância, sem evidência de efeito tóxico e inflamação significativa.
Em outro trabalho, desenvolveu-se um implante biodegradável contendo doxorrubicina para o tratamento de vitreorretinopatia proliferativa experimental em coelhos e a taxa de liberação da droga no humor vítreo foi avaliada(12). Esse sistema era composto de PLGA, contendo 1% de doxorrubicina e foi implantado na pars plana, sendo capaz de promover a liberação diretamente no vítreo e não alterando a transparência do meio ocular. As concentrações da droga no local de liberação, após o implante, foram medidas. Os estudos in vitro apresentaram resultados de liberação de 26% da droga durante quatro semanas, e os in vivo mostraram uma manutenção da concentração dessa no humor vítreo dentro da faixa terapêutica por um período superior a quatro semanas. Não foi observada nenhuma reação tóxica significativa após realização de eletrorretinografia e histopatologia do local. A partir dos resultados obtidos, os pesquisadores acreditam que sistemas constituídos por polímeros biodegradáveis se tornem bastante promissores no que diz respeito à liberação controlada de drogas no vítreo.
Foi estudada igualmente, a eficácia de um implante à base de PLGA, contendo 5-fluorouracila (5-FU), para o tratamento de PVR(13). As concentrações intravítreas da droga foram mantidas entre 1,0 e 13,0 µg/mL por, no mínimo, 14 dias, e permaneceram acima de 0,3 µg/mL por cerca de 21 dias. A implantação do sistema se mostrou eficaz na inibição de PVR, sem sinais de efeitos tóxicos na retina.
Um implante escleral capaz de liberar a droga no vítreo foi desenvolvido por diversos pesquisadores(15). Esse sistema foi preparado com PLA e PLGA, utilizando diferentes concentrações da droga, o ganciclovir, e foram testados em coelhos para o tratamento de CMVR. Os estudos de liberação in vitro mostraram que a degradação do PLGA era influenciada pela composição dos ácidos lático e glicólico, sendo que quanto maior a fração glicolítica, mais rápida era a taxa de degradação. Embora os implantes de PLA tenham liberado a droga por seis meses, esses não apresentaram aplicação terapêutica já que obtiveram um longo período de latência. Para os estudos de liberação in vivo e de biodegradação, foram utilizados, portanto, os dispositivos de PLGA 75:25. Os resultados observados mostraram que a concentração da droga foi mantida dentro da faixa terapêutica para humanos, no vítreo, por mais de três meses e na retina/coróide por mais de cinco meses. No estudo de biodegradação, todos os sistemas desapareceram do vítreo e do espaço subconjuntival cinco meses após terem sido implantados.
No sentido de melhorar o perfil de liberação dos implantes acima estudados, foi desenvolvido outro trabalho pelo mesmo grupo, utilizando sistemas à base de misturas de PLA de peso molecular alto e baixo(24). Os resultados in vitro mostraram que o implante composto de PLA (70000 Daltons) e PLA (5000 Daltons) na proporção de 80/20 foi o mais adequado, sendo, então, utilizado nos estudos in vivo. A concentração de ganciclovir no vítreo foi mantida dentro da faixa terapêutica por 6 meses a partir desse implante.
Zhou e colaboradores desenvolveram um implante para o tratamento de PVR, composto de PLGA 50:50, contendo três segmentos cilíndricos, cada um contendo uma das seguintes drogas: 5-fluorouridina (5-FUrd), triamcinolona (Triam) e um agente trombolítico (t-PA)(14). No segmento de t-PA, o implante foi revestido com PLGA, no sentido de promover um período de latência para liberação da droga no momento adequado e, também, para reduzir o risco de sangramento pós-operatório. Conseguiu-se combinar todos os três segmentos, e o pro-cesso de revestimento foi bem sucedido, produzindo-se, então, os implantes. Os resultados mostraram que o 5-FUrd e o Triam foram liberados na taxa de 1,0 µg/dia por mais de quatro semanas e de 10,0-190,0 µg/dia por mais de duas semanas, respectivamente. Após um período de latência de cerca de dois dias, o t-PA foi liberado ativo na taxa de 0,2-0,5 mg/dia durante duas semanas.
Recentemente, têm sido realizados estudos de um sistema de liberação de dexametasona para o tratamento de inflamação após cirurgia de catarata(25-26). Esse implante foi preparado com PLGA e continha 60 mg da droga. O sistema foi capaz de promover liberação da droga por um período de, aproximadamente, 7-10 dias. Os estudos clínicos revelaram, ainda, que o implante foi bem tolerado e efetivo contra a inflamação.
PERSPECTIVAS
O tratamento de doenças do segmento posterior do olho é limitado devido à dificuldade de acesso aos tecidos dessa região; a obtenção de níveis terapêuticos desejáveis, através das vias convencionais de administração, é praticamente impossível. A barreira hemato-ocular atua como um mecanismo protetor contra substâncias exógenas, que incluem as drogas.
A administração tópica, na forma de soluções, suspensões, géis e pomadas, apresenta um efeito terapêutico praticamente insignificante nas estruturas posteriores do olho. As drogas utilizadas pela via sistêmica também penetram muito pouco no olho e, algumas vezes, é necessário o tratamento prolongado com doses elevadas, através de injeções intravenosas, para manutenção da concentração no vítreo dentro da faixa terapêutica, o que pode ocasionar sérios efeitos adversos. A administração intravítrea seria uma alternativa para que se atinja uma concentração elevada da droga nos tecidos oculares posteriores. Entretanto, geralmente, são requeridas injeções repetidas nesse local, que podem resultar em inúmeras complicações e desconforto para o paciente.
Sistemas de liberação controlada tornam-se, dessa forma, essenciais para o tratamento de doenças oculares.
Os materiais poliméricos desempenham um papel importante na taxa de liberação e os do tipo biodegradáveis, principalmente, têm sido extensamente investigados nas últimas décadas para aplicação em sistemas de liberação controlada destinados à via ocular. Esses materiais podem promover um aumento da biodisponibilidade e uma redução de efeitos adversos, desde que a biocompatibilidade do polímero no olho, que é um importante fator para a aplicação clínica, seja avaliada.
Para o tratamento de doenças do segmento posterior do olho, em que são necessárias administrações intra-oculares freqüentes, o desenvolvimento de implantes de liberação prolongada de drogas se torna, portanto, promissor e constitui um dos campos mais pesquisados em terapêutica oftálmica atualmente.
Estudos visando a obtenção de implantes biodegradáveis contendo antiinflamatórios esteróides para o tratamento de uveítes estão, atualmente, sendo realizados na Faculdade de Farmácia da UFMG em colaboração com o Serviço de Retina e Vítreo do Hospital das Clínicas da Faculdade de Medicina de Ribeirão Preto da Universidade de São Paulo.
REFERÊNCIAS
1. Kimura H, Ogura Y. Biodegradable polymers for ocular drug delivery. Ophthalmologica 2001;215:143-55.
2. Yasukawa T, Kimura H, Tabata Y, Ogura Y. Biodegradable scleral plugs for vitreoretinal drug delivery. Adv Drug Deliv Rev 2001;52:25-36.
3. Colthurst MJ, Williams RL, Hiscott PS, Grierson I. Biomaterials used in the posterior segment of the eye. Biomaterials 2000;21:649-65.
4. Peyman GA, Ganiban GJ. Delivery systems for intraocular routes. Adv Drug Deliv Rev 1995;16:107-23.
5. Athanasiou KA, Niederauer GG, Agrawal CM. Sterilization, toxicity, biocompatibility and clinical applications of polylactic acid/polyglycolic acid copolymers. Biomaterials 1996;17:93-102.
6. Dash AK, Cudworth GC. Therapeutic applications of implantable drug delivery systems. J Pharmacol Toxicol Methods 1998;40:1-12.
7. Jain R, Shah NH, Malick AW, Rhodes CT. Controlled drug delivery by biodegradable poly (ester) devices: different preparative approaches. Drug Dev Ind Pharm 1998;24:703-27.
8. Merkli A, Tabatabay C, Gurny R, Heller J. Biodegradable polymers for the controlled release of ocular drugs. Prog Polym Sci 1998;23:563-80.
9. Jain RA. The manufacturing techniques of various drug loaded biodegradable poly (lactide-co-glycolide) (PLGA) devices. Biomaterials 2000;21:2475-90.
10. Blanco-Prieto MJ, Fattal E, Puisieux F, Couvreur P. The multiple emulsion as a common step for the design of polymeric microparticles. In: Grossiord JL, Seiller M. Multiple emulsions: structure, properties and applications. França: Éditions de Santé; 1998. p.397-435.
11. Lewis DH. Controlled release of bioactive agents from lactide/glycolide polymers. In: Chasin M, Langer R. Biodegradable polymers as drug delivery systems. New York: Marcel Dekker; 1990. p.01-41.
12. Hashizoe M, Ogura Y, Kimura H, Moritera T, Honda Y, Kyo M, Hyon SH, Ikada Y. Scleral plug of biodegradable polymers for controlled drug release in the vitreous. Arch Ophthalmol 1994;112:1380-4.
13. Rubsamen PE, Davis PA, Hernandez E, O'Grady GE, Cousins SW. Prevention of experimental proliferative vitreoretinopathy with a biodegradable intravitreal implant for the sustained release of fluorouracil. Arch Ophthalmol 1994;112:407-13.
14. Zhou T, Lewis H, Foster RE, Schwendeman SP. Development of a multiple-drug delivery implant for intraocular management of proliferative vitreoretino- pathy. J Control Release 1998;55:281-95.
15. Kunou N, Ogura Y, Hashizoe M, Honda Y, Hyon SH, Ikada Y. Controlled intraocular delivery of ganciclovir with use of biodegradable scleral implant in rabbits. J Controlled Rel 1995;37:143-50.
16. Results of the Endophthalmitis Vitrectomy Study. A randomized trial of immediate vitrectomy and of intravenous antibiotics for the treatment of postoperative bacterial endophthalmitis. Endophthalmitis Vitrectomy Study Group. Arch Ophthalmol 1995;113:1479-96.
17. Cheng CK, Berger AS, Pearson PA, Ashton P, Jaffe GJ. Intravitreal sustained-release dexamethasone device in the treatment of experimental uveitis. Invest Ophthalmol Vis Sci 1995;36:442-53.
18. Jonas JB, Kreissig I, Degenring R. Repeated intravitreal injections of triamcinolone acetonide as treatment of progressive exudative age-related macular degeneration. Graefes Arch Clin Exp Ophthalmol 2002;240:873-4.
19. Penfold PL, Gyory JF, Hunyor AB, Billson FA. Exudative macular degeneration and intravitreal triamcinolone. A pilot study. Aust N Z J Ophthalmol 1995;23:293-8.
20. Martidis A, Duker JS, Greenberg PB, Rogers AH, Puliafito CA, Reichel E, Baumal C. Intravitreal triamcinolone for refractory diabetic macular edema. Ophthalmology 2002;109:920-7.
21. Conway MD, Canakis C, Livir-Rallatos C, Peyman GA. Intravitreal triamci- nolone acetonide for refractory chronic pseudophakic cystoid macular edema. J Cataract Refract Surg 2003;29:27-33.
22. Yang CS, Khawly JA, Hainsworth DP, Chen SN, Ashton P, Guo H, Jaffe GJ. An intravitreal sustained-release triamcinolone and 5-fluorouracil codrug in the treatment of experimental proliferative vitreoretinopathy. Arch Ophthalmol 1998;116:69-77.
23. Kimura H, Ogura Y, Hashizoe M, Nishiwaki H, Honda Y, Ikada Y. A new vitreal drug delivery system using an implantable biodegradable polymeric device. Invest Ophthalmol Vis Sci 1994;35:2815-9.
24. Kunou N, Ogura Y, Yasukawa T, Kimura H, Miyamoto H, Honda Y, Ikada Y. Long-term sustained release of ganciclovir from biodegradable scleral implant for the treatment of cytomegalovirus retinitis. J Control Release 2000; 68:263-71.
25. Tan DT, Chee SP, Lim L, Lim AS. Randomized clinical trial of a new dexamethasone delivery system (Surodex) for treatment of post-cataract surgery inflammation. Ophthalmology 1999;106:223-31.
26. Tan DT, Chee SP, Lim L, Theng J, Van Ede M. Randomized clinical trial of Surodex steroid drug delivery system for cataract surgery: anterior versus posterior placement of two Surodex in the eye. Ophthalmology 2001;108: 2172-81.
Endereço para correspondência
Av. Olegário Maciel, 2360
Belo Horizonte (MG) CEP 30180-112
E-mail: [email protected]
Recebido para análise em 04.06.2003
Versão revisada recebida em 06.10.2003
Aprovação em 18.11.2003